题目内容
(7分)有一硝酸盐晶体,其化学式为M(NO3)x·yH2O,相对分子质量为242。取1.21g该晶体溶于水,配成100mL溶液,将此溶液用石墨作电极进行电解,当有0.01mol电子发生转移时,溶液中金属全部析出。经称量阴极增重0.32g。求:
(1)金属M的相对原子质量及x、y。
(2)电解后溶液的pH(电解过程中溶液体积变化忽略不计)。
(7分)(M)=n[M(NO3)x·yH2O]=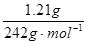 =0.005mol
=0.005mol
![]() M的化合价=
M的化合价=![]() 所以x=2
所以x=2
根据64+2(14+48)+18y=242 得y=3
(2)电解总反应为: 2M(NO3)2+2H2O 2M + 4HNO3 +O2↑
2 4
0.005mol n
n(HNO3)=![]()
![]()
pH = -lg10--1 = 1
解析:

练习册系列答案
相关题目
 有一硝酸盐晶体,其化学式表示为M(NO3)x?nH2O经测定其摩尔质量为242g?mol-1.取1.21g该晶体溶于水配成100mL溶液.将此溶液倒入右图所示装置中,用石墨作电极进行电解.当有0.01mol电子通过电极时,溶液中的金属阳离子全部析出,在A极得到金属0.32g.回答:
有一硝酸盐晶体,其化学式表示为M(NO3)x?nH2O经测定其摩尔质量为242g?mol-1.取1.21g该晶体溶于水配成100mL溶液.将此溶液倒入右图所示装置中,用石墨作电极进行电解.当有0.01mol电子通过电极时,溶液中的金属阳离子全部析出,在A极得到金属0.32g.回答: