题目内容
![]() (10分)CO是一种无色、无味且不溶于水的有毒气体,其制法有:
(10分)CO是一种无色、无味且不溶于水的有毒气体,其制法有:
![]() (1)实验室可用甲酸和浓
(1)实验室可用甲酸和浓![]() 共热制取CO.
共热制取CO.
![]()
![]()
![]() a.甲酸和浓
a.甲酸和浓![]() 应怎样混合?浓
应怎样混合?浓![]() 起什么作用?
起什么作用?
![]()
![]() b.请据实验原理选择所需主要玻璃仪器(导管除外).
b.请据实验原理选择所需主要玻璃仪器(导管除外).
![]()
![]() c.怎样收集CO气体?
c.怎样收集CO气体?
![]() (2)实验室还可用草酸晶体与浓
(2)实验室还可用草酸晶体与浓![]() 共热制取CO.
共热制取CO.
![]()
![]()
![]() 请问:怎样才能得到不含
请问:怎样才能得到不含![]() 的CO气体?
的CO气体?
![]()
![]() (3)工业上用焦炭和水在高温下发生反应制取CO,其化学方程式为:____________
(3)工业上用焦炭和水在高温下发生反应制取CO,其化学方程式为:____________
![]() ____.在此条件下,C和
____.在此条件下,C和![]() 的还原性谁强?
的还原性谁强?
解析:
(1)a.将甲酸滴入热的浓![]() 中.脱水作用. b.分液漏斗(装甲酸)、圆底烧瓶(装浓
中.脱水作用. b.分液漏斗(装甲酸)、圆底烧瓶(装浓![]() )、酒精灯、干燥管、集气瓶. c.用排水法收集.
)、酒精灯、干燥管、集气瓶. c.用排水法收集.
![]() (2)通过碱石灰或NaOH溶液. (3)
(2)通过碱石灰或NaOH溶液. (3)![]() 还原性(
还原性(![]() ).
).

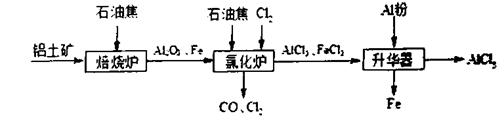
![]() 钛呈银白色,因它坚硬、强度大、耐热、密度小,被称为高技术金属。目前生产钛采用氯化法,即将金红石或钛铁矿与焦炭混合,通入氯气并加热制得TiCl4:
钛呈银白色,因它坚硬、强度大、耐热、密度小,被称为高技术金属。目前生产钛采用氯化法,即将金红石或钛铁矿与焦炭混合,通入氯气并加热制得TiCl4:
![]() 2FeTiO3+7Cl2+6C 2TiCl4+2FeCl3+6CO
2FeTiO3+7Cl2+6C 2TiCl4+2FeCl3+6CO
TiO2+2Cl2+2C TiCl4+2CO
![]() 将TiCl4蒸馏并提纯,在氩气保护下与镁共热得到钛:
将TiCl4蒸馏并提纯,在氩气保护下与镁共热得到钛:
TiCl4+2Mg Ti+2MgCl2
MgCl2和过量Mg用稀盐酸溶解后得海绵状钛,再在真空熔化铸成钛锭。
请回答下列问题:
(1)基态钛原子的价电子排布式为 。
(2)与CO互为等电子体的离子为 (填化学式)。
(3)在CH2Cl2、C6H6、CO2、C2H4中,碳原子采取sp1杂化的分子有 。
(4)TiCl4在常温下是无色液体,在水或潮湿空气中易水解而冒白烟。则TiCl4属于
(填“原子”、“分子”或“离子”)晶体。
|
(6)在自然界中TiO2有金红石、板钛矿、锐钛矿三种晶型,其
中金红石的晶胞如右图所示,则其中Ti4+的配位数为 。
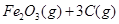
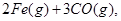
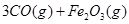

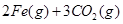 。则反应②的平衡常数的表达式为K= 。
。则反应②的平衡常数的表达式为K= 。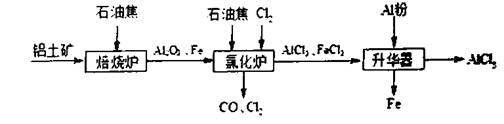
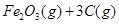

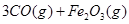

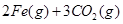 。则反应②的平衡常数的表达式为K=
。
。则反应②的平衡常数的表达式为K=
。