题目内容
(11分)能源可划分为一次能源和二次能源。自然界中以现成形式提供的能源称为一次能源;需依靠其他能源的能量间接制取的能源称为二次能源。氢气是一种高效而没有污染的二次能源,它可以由自然界中大量存在的水来制取:2H2O(l)===2H2(g)+O2(g) ΔH=+571.6 kJ/mol。根据以上叙述回答:
(1)下列叙述正确的是 。(不定项选择)(4分)
A.电能是二次能源 B.水力是二次能源
C.天然气是一次能源 D.焦炉气是一次能源
(2)已知:CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890.3 kJ/mol,等质量的氢气和甲烷分别完全燃烧后,放出的热量之比约为( )(3分)
A.1∶3.4 B.1∶1.7 C.2.6∶1 D.4.6∶1
(3)关于用水制取二次能源氢气,以下研究方向不正确的是 。(不定项选择)(4分)
A.组成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二次能源
B.设法将太阳光聚焦,产生高温,使水分解产生氢气
C.寻找高效催化剂,使水分解产生氢气,同时释放能量
(1)AC (2)C (3)AC
【解析】(1)一次能源,也称天然能源,是指从自然界取得未经改变或转变而直接利用的能源。如原煤、原油、天然气、水能、风能、太阳能、海洋能、潮汐能、地热能、天然铀矿等。二次能源是指由一次能源经过加工转换以后得到的能源,例如:电力、蒸汽、煤气等等。所以AC正确,水力是一次能源,焦炉气是二级能源,答案选AC。
(2)根据热化学方程式可知,等质量的氢气和甲烷分别完全燃烧后,放出的热量之比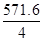 ︰
︰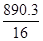 =
=
2.6︰1,答案选C。
(3)氧气是助燃的,A不正确;水分解是吸热反应,C不正确,所以答案选AC。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案材料一:酸雨是英国化学家R.A.Smith 1872年最先提出的,一般是指pH小于5.6的雨、雪、雾等大气降水,是大气污染的表现。酸雨被称作“空中死神”。据某市区1998年环境状况公报载,市区酸雨频率为41.3%,比上年上升了5.5个百分点。降水的年平均pH为4.87,降水酸性污染较严重,表现为煤烟型污染特征。
材料二:①某地一场较大范围的酸雨使植物叶面遭到腐蚀,产生大量斑点而坏死,导致西瓜大面积绝产,损失惨重。②酸雨使植物阳离子从叶面析出,使钙、镁、铁等离子迅速从土壤中损失,土壤营养状况降低,还使光合作用受到抑制,影响植物的生长。③铝对生物来说是有害元素,在土壤中以氧化铝形式存在,pH=5.6时几乎不溶解。当pH为4.6时,铝的溶解度增加100倍,并转化成硫酸铝,造成树木死亡。四川某林场,华山松死亡率达96%,就是酸雨使土壤中硫酸铝浓度增高,危及华山松。
材料三:我国农业生产因遭受酸雨造成的损失每年高达15亿元。为了有效控制酸雨,国务院已经批准了《酸雨控制区和二氧化硫控制区划分方案》等规定。
某研究性学习小组计划研究当地酸雨的形成过程,于是取来雨水作水样进行测定,随时间的推移,多次测定该样品的pH,得到如下数据:
时间/h | 开始 | 8 | 16 | 24 | 32 | 40 | 48 |
pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
(1)问题:①雨水样品放置时pH变化的主要原因(用化学方程式表示)_____________________;由此可以得出酸雨的形成过程可能是______________________________________________。
②如果将刚取样的上述雨水和自来水相混合,pH将_________________ (填“增大”“减小”或“不变”),原因是__________________________________;二氧化硫表现_____________性。
(2)列举酸雨给人类造成的危害。
(3)你认为减少酸雨产生的途径可采取的下列措施是__________________________________。
①少用煤作燃料 ②把工厂的烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
A.①③ B.②③④⑤ C.①③⑤ D.①③④⑤
(4)为了减少煤燃烧时向大气排放的二氧化硫,不同的地方往往采取不同的“固硫”方法。
①火力发电厂常用Ca(OH)2的悬浊液吸收煤燃烧时产生的二氧化硫气体,并回收制得有用的石膏(CaSO4·2H2O),则有关反应的化学方程式_____________________,__________________,___________________。
②硫酸工业常用浓氨水来吸收二氧化硫,则有关的化学方程式为_____________________。
③有些工业采取将生石灰和含硫煤混合使用。请写出燃烧时有关“固硫”反应的化学方程式。__________________________________________
④国际上最新采用“饱和亚硫酸钠溶液吸收SO2法”。请写出有关反应的化学方程式。_____________________
⑤请比较以上四种“固硫”方法的优缺点。_____________________
试根据下述材料完成问题:
材料一:酸雨是英国化学家R.A.Smith 1872年最先提出的,一般是指pH小于5.6的雨、雪、雾等大气降水,是大气污染的表现。酸雨被称作“空中死神”。据某市区1998年环境状况公报载,市区酸雨频率为41.3%,比上年上升了5.5个百分点。降水的年平均pH为4.87,降水酸性污染较严重,表现为煤烟型污染特征。
材料二:①某地一场较大范围的酸雨使植物叶面遭到腐蚀,产生大量斑点而坏死,导致西瓜大面积绝产,损失惨重。②酸雨使植物阳离子从叶面析出,使钙、镁、铁等离子迅速从土壤中损失,土壤营养状况降低,还使光合作用受到抑制,影响植物的生长。③铝对生物来说是有害元素,在土壤中以氧化铝形式存在,pH=5.6时几乎不溶解。当pH为4.6时,铝的溶解度增加100倍,并转化成硫酸铝,造成树木死亡。四川某林场,华山松死亡率达96%,就是酸雨使土壤中硫酸铝浓度增高,危及华山松。
材料三:我国农业生产因遭受酸雨造成的损失每年高达15亿元。为了有效控制酸雨,国务院已经批准了《酸雨控制区和二氧化硫控制区划分方案》等规定。
某研究性学习小组计划研究当地酸雨的形成过程,于是取来雨水作水样进行测定,随时间的推移,多次测定该样品的pH,得到如下数据:
| 时间/h | 开始 | 8 | 16 | 24 | 32 | 40 | 48 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
问题:①雨水样品放置时pH变化的主要原因(用化学方程式表示)_____________________;由此可以得出酸雨的形成过程可能是
______________________________________________。
②如果将刚取样的上述雨水和自来水相混合,pH将_________________ (填“增大”“减小”或“不变”),原因是__________________________________;二氧化硫表现_____________性。
(2)列举酸雨给人类造成的危害。
(3)你认为减少酸雨产生的途径可采取的下列措施是
__________________________________。
①少用煤作燃料 ②把工厂的烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
A.①③ B.②③④⑤ C.①③⑤ D.①③④⑤
(4)为了减少煤燃烧时向大气排放的二氧化硫,不同的地方往往采取不同的“固硫”方法。
①火力发电厂常用Ca(OH)2的悬浊液吸收煤燃烧时产生的二氧化硫气体,并回收制得有用的石膏(CaSO4·2H2O),则有关反应的化学方程式_____________________,
__________________,___________________。
②硫酸工业常用浓氨水来吸收二氧化硫,则有关的化学方程式为_____________________。
③有些工业采取将生石灰和含硫煤混合使用。请写出燃烧时有关“固硫”反应的化学方程式。
④国际上最新采用“饱和亚硫酸钠溶液吸收SO2法”。请写出有关反应的化学方程式。
⑤请比较以上四种“固硫”方法的优缺点。