题目内容
【题目】研究钠及其化合物有重要意义。
(1)实验室配制0.1molL-1的碳酸钠溶液480mL,根据配制溶液的过程,回答问题:
①实验中除需要托盘天平(带砝码)、药匙、烧杯和玻璃棒外,还需要的其他玻璃仪器是_________。
②实验中需用托盘天平(带砝码)称量碳酸钠固体_______________g。
③某同学配制 Na2CO3溶液的过程如图所示。你认为该同学的错误有___________。
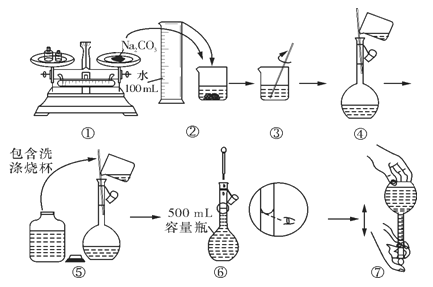
A.①⑥ B.②④⑦ C.①⑤⑥ D.⑤⑥⑦
④下列实验操作会使配得的溶液浓度偏小的是___________。
A.转移溶液后未洗涤烧杯和玻璃棒就直接定容
B.容量瓶使用前没有经过干燥,瓶中有少量的水
C.在容量瓶中定容时俯视刻度线
D.定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水至刻度
(2)过氧化钠保存不当容易变质生成Na2CO3。某过氧化钠样品已经部分变质,请你设计实验,限用一种溶液和水,证明过氧化钠已经部分变质:_________________(说明操作、现象和结论)。
【答案】 500mL容量瓶、胶头滴管 5.3 A AD 取少量样品于一洁净试管中,加水溶解,向其中加入BaCl2(或CaCl2)溶液,充分振荡,有白色沉淀生成,证明Na2O2已经变质
【解析】(1)①要配制0.1molL-1的碳酸钠溶液480mL,实验室没有480mL的容量瓶,需要选用500mL的容量瓶,配制步骤为:计算、称量、溶解、冷却、转移、洗涤、定容、摇匀等,需要使用的仪器有:托盘天平、玻璃棒、烧杯、药匙、500mL容量瓶、胶头滴管等,还缺少的玻璃仪器为:500mL容量瓶、胶头滴管。
故答案为:500mL容量瓶;胶头滴管;
②依据m=CVM,需要Na2CO3的质量=0.1molL1×0.5L×106g/mol=5.3g;
故答案为:5.3;
③、操作①中称量Na2CO3质量,药品与砝码位置颠倒,正确方法应该为“左物右码”,否则导致称量的碳酸钠质量偏小,故①错误;操作②、③为溶解Na2CO3,使用玻璃棒搅拌,加速溶解过程,操作正确,故②③正确;步骤④为转移冷却后的碳酸钠溶液,需要使用玻璃棒引流,玻璃棒下端放到容量瓶刻度线一下,过程正确,故④正确;步骤⑤为转移洗涤烧杯、和玻璃棒的溶液,该操作正确,故⑤正确;操作⑥为使用胶头滴管定容,定容时眼睛应该与容量瓶刻度线平视,不能仰视刻度线,故⑥错误;操作⑦为摇匀操作,摇匀时应该上下颠倒充分摇匀,故⑦正确;所以以上错误操作有①⑥,故选A。
④A、转移溶液后,未洗涤烧杯和玻璃棒就直接定容,会导致溶质n偏小,溶液浓度偏小,故A正确;B、溶解后立即转移,由于Na2CO3溶于水放热,热胀冷缩,导致溶液V减小,浓度偏大,故B错误;C、进行定容时,俯视刻度线,会导致溶液体积偏小,浓度偏大,故C错误;D、定容且把容量瓶倒置摇匀后,发现液面下降,此时有少量溶液残留在玻璃塞和瓶口之间,浓度不变,属于正常现象,但又补充了水,会导致浓度偏小,故D正确。故答案为:AD。
Na2O2保存不当容易变质,生成Na2CO3,所以检查Na2O2是否变质,只需检验CO32-,选用BaCl2溶液,方法是取少量样品,溶解,加入BaCl2(或CaCl2)溶液,充分振荡,有白色沉淀,证明Na2O2已经变质。
故答案为:取少量样品于一洁净试管中,加水溶解,向其中加入BaCl2(或CaCl2)溶液,充分振荡,有白色沉淀生成,证明Na2O2已经变质。

 阅读快车系列答案
阅读快车系列答案