题目内容
传统合成氨工业需要采用高温、高压和催化剂.近来美国化学家使用新型催化剂,在常温下合成了氨气.下列说法正确的是( )
| A、传统合成氨方法的△H>0,新型合成氨方法的△H<0 |
| B、新型合成氨方法不需高温,符合节能减排的生产理念 |
| C、新型催化剂提高了N2和H2的转化率 |
| D、两种方法的化学平衡常数相同 |
考点:化学平衡的调控作用
专题:化学平衡专题
分析:A.根据盖斯定律可知,反应过程中吸收、放出的热量与反应途径无关,所以两种合成氨的焓变相同,都一定是放热反应;
B.在常温常压下合成出氨,可节约大量能源,能够节能减排;
C.使用催化剂能够改变反应速率,但是不会影响化学平衡,所以催化剂不会改变当前和氢气的转化率;
D.化学平衡常数受反应温度的影响,反应温度不同,化学平衡常数则不同.
B.在常温常压下合成出氨,可节约大量能源,能够节能减排;
C.使用催化剂能够改变反应速率,但是不会影响化学平衡,所以催化剂不会改变当前和氢气的转化率;
D.化学平衡常数受反应温度的影响,反应温度不同,化学平衡常数则不同.
解答:
解:A.反应热与反应途径无关,所以旧法合成氨与新法合成氨都是放热反应,故A错误;
B.与旧法相比较,新法合成氨不需要在高温条件下,可节约大量能源,具有发展前景,符合节能减排的生产理念,故B正确;
C.催化剂只能改变反应速率,对反应物的转化率没有影响,所以新型催化剂不会提高N2和H2的转化率,故C错误;
D.化学平衡常数与反应温度有关,两种方法的反应温度不同,则化学平衡常数一定不同,故D错误;
故选B.
B.与旧法相比较,新法合成氨不需要在高温条件下,可节约大量能源,具有发展前景,符合节能减排的生产理念,故B正确;
C.催化剂只能改变反应速率,对反应物的转化率没有影响,所以新型催化剂不会提高N2和H2的转化率,故C错误;
D.化学平衡常数与反应温度有关,两种方法的反应温度不同,则化学平衡常数一定不同,故D错误;
故选B.
点评:本题考查了化学平衡及其影响因素,题目难度中等,注意掌握温度、难度、催化剂等对化学平衡的影响,明确催化剂不会影响化学平衡及反应物的转化率、化学平衡常数与温度相关,温度不同,则化学平衡常数不同.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
给试管中某红色溶液加热,溶液颜色逐渐变浅,则原溶液可能是( )
①滴有石蕊的NH4Cl溶液 ②滴有酚酞的氨水溶液 ③滴有石蕊的H2SO4溶液
④滴有酚酞的饱和氢氧化钙溶液 ⑤滴有酚酞的Na2CO3溶液 ⑥溶有SO2的品红溶液.
①滴有石蕊的NH4Cl溶液 ②滴有酚酞的氨水溶液 ③滴有石蕊的H2SO4溶液
④滴有酚酞的饱和氢氧化钙溶液 ⑤滴有酚酞的Na2CO3溶液 ⑥溶有SO2的品红溶液.
| A、②④ | B、①③⑤ |
| C、①④⑥ | D、②③ |
下列有关甲烷和苯的说法,正确的是( )
| A、都可以用家庭燃料 |
| B、都可以与氢气发生加成反应 |
| C、都可以被酸性高锰酸钾溶液氧化 |
| D、都可以与氯气发生取代反应 |
使用一种试剂就能鉴别出来的一组物质是( )
| A、甲苯 己烯 苯 乙醇 |
| B、甲苯 己烯 CCl4 乙醇 |
| C、硝基苯 苯 溴乙烷 乙醇 |
| D、苯 甲苯 二甲苯 乙醇 |
将NH4NO3加热反应,有N2、HNO3和H2O生成,配平后的方程式中计量系数由小到大的顺序是( )
| A、NH4NO3、N2、HNO3、H2O |
| B、HNO3、N2、NH4NO3、H2O |
| C、H2O、NH4NO3、N2、HNO3 |
| D、N2、NH4NO3、HNO3、H2O |
以下储存物质的方法正确的是( )
| A、少量钠储存在酒精中 |
| B、氢氧化钠溶液存放在带有橡皮塞的细口瓶中 |
| C、少量硫磺存放在二硫化碳中 |
| D、液溴存放在带有橡皮塞的棕色细口瓶中 |
2003年春,北京小汤山等收治“非典”的定点医院,收到由解放军总装备部军事医学研究所研制的小分子团水,解决了医务人员工作时的如厕难题.新型小分子团“压缩”水,具有饮用量少、渗透力强、生物利用率高、在人体内储留时间长、排放量少的特点.一次饮用125mL小分子团水,可维持人体6小时正常需水量.下列关于小分子团水的说法正确的是( )
| A、水分子的化学性质发生了改变 |
| B、水分子中氧氢键数目增多 |
| C、水分子团中水分子间的作用力为分子间作用力 |
| D、水分子的结构、物理性质发生了改变 |
下列关于元素周期表的说法中,错误的是( )
| A、元素周期表是元素按原子序数从小到大排列而成的 |
| B、元素原子的电子层数等于其所在周期的周期序数 |
| C、四、五、六周期中都含有18种元素 |
| D、元素周期表中有18列、16个族 |
 ⑧
⑧
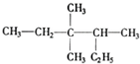
 ?2,2-二甲基丁烷.
?2,2-二甲基丁烷.