题目内容
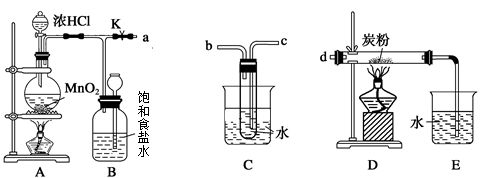
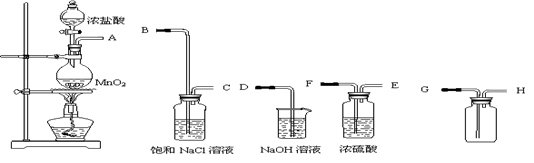
用MnO2和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水CuCl2,装置如下图所示。
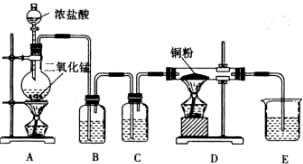
请回答下列问题:
(1)A 中发生反应的化学方程式为
(2)B中选用的试剂是饱和食盐水,其作用是除去Cl2中的杂质 ;C中选用的试剂是 ,其作用是除去Cl2中的
(3)E装置发生反应的离子方程式是
(4)用含HCl 14.6g的浓盐酸与足量的MnO2反应产生氯气的物质的量应______0.1mol(填大于、小于或等于)

请回答下列问题:
(1)A 中发生反应的化学方程式为
(2)B中选用的试剂是饱和食盐水,其作用是除去Cl2中的杂质 ;C中选用的试剂是 ,其作用是除去Cl2中的
(3)E装置发生反应的离子方程式是
(4)用含HCl 14.6g的浓盐酸与足量的MnO2反应产生氯气的物质的量应______0.1mol(填大于、小于或等于)
(10分)(1)MnO2+4HCl(浓) MnCl2+Cl2↑+ H2O
MnCl2+Cl2↑+ H2O
(2)HCl 浓硫酸 水蒸气
(3)Cl2+2OH-==Cl- +ClO- + H2O
(4)<
 MnCl2+Cl2↑+ H2O
MnCl2+Cl2↑+ H2O(2)HCl 浓硫酸 水蒸气
(3)Cl2+2OH-==Cl- +ClO- + H2O
(4)<
试题分析:(1)A装置是制取Cl2,化学方程式为MnO2+4HCl(浓)
 MnCl2+Cl2↑+ H2O。
MnCl2+Cl2↑+ H2O。(2) 饱和食盐水除去HCl;C装置的作用是干燥Cl2,用的是浓硫酸,其作用是除去Cl2中的水蒸气。
(3)E装置是吸收多余的Cl2,离子方程式是Cl2+2OH-==Cl- +ClO- + H2O。
(4)反应过程中浓盐酸的浓度越来越稀,就不反应生成Cl2,故用含HCl 14.6g的浓盐酸与足量的MnO2反应产生氯气的物质的量应小于0.1mol。
点评:本题考查了气体的制取、净化、检验、收集、尾气处理装置,制取气体的反应装置类型有:固体、固体加热型,如制取氨气;固体、液体加热型,如制取氯气;固体、液体不加热型,如制取氢气等,根据反应物的状态、条件选择不同的反应装置。

练习册系列答案
 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目