题目内容
I.已知四种强电解质溶液,分别含有下列阴、阳离子中的各一种,并且互不重复:NH4+、Ba2+、Na+、H+、SO42-、NO3-、OH-、CO32-.将这四种溶液分别标记为A、B、C、D,进行如下实验:
①在A或D中滴入C,均有沉淀生成;②D和B反应生成的气体能被A吸收;③A和D反应生成的气体能被B吸收.
写出化学式:A
Ⅱ.已知下列信息:
(CH3)2C=CHCH3
CH3- -CH3+CH3COOH
-CH3+CH3COOH
CH2=CH-CH=CH2+CH2=CH2

一种用途较广泛的有机玻璃树脂--聚丁烯酸甲酯结构简式为: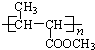
有一种合成这种高聚物的途径副产物污染少或无污染,原子利用率较高,符合“绿色化学挑战计划”的要求,其合成路线如下:

试回答下列问题:
(1)写出B、D的结构简式:B
 ,D
,D
 ;
;
(2)反应④属于
(3)在上述合成过程中,原子利用率最高的化学反应有
①在A或D中滴入C,均有沉淀生成;②D和B反应生成的气体能被A吸收;③A和D反应生成的气体能被B吸收.
写出化学式:A
H2SO4
H2SO4
,CBa(NO3)2
Ba(NO3)2
.Ⅱ.已知下列信息:
(CH3)2C=CHCH3
| KMnO4 |
| H+ |
 -CH3+CH3COOH
-CH3+CH3COOHCH2=CH-CH=CH2+CH2=CH2
| 120℃ |

一种用途较广泛的有机玻璃树脂--聚丁烯酸甲酯结构简式为:
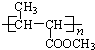
有一种合成这种高聚物的途径副产物污染少或无污染,原子利用率较高,符合“绿色化学挑战计划”的要求,其合成路线如下:

试回答下列问题:
(1)写出B、D的结构简式:B




(2)反应④属于
消去(或脱水)
消去(或脱水)
反应(填反应类型);(3)在上述合成过程中,原子利用率最高的化学反应有
①③⑥
①③⑥
(填编号).分析:Ⅰ.这种题目的突破口在A或D中滴入C,均有沉淀生成,C中一定有Ba2+,D和A、B都能生成气体,根据分别含有下列阴、阳离子中的各一种,并且互不重复,利用离子之间的反应与离子共存来分析.
Ⅱ:采取逆推法,抓住碳链骨架的变化及官能团的变化及性质,并根据反应条件判断反应类型和相关物质.如转化关系中反应条件是KMnO4,我们就想到是氧化反应,再结合题干信息,便知是双键断裂;看到反应条件浓H2SO4,便猜测消去反应或酯化反应,再结合前后转化关系,得出正确结论.
Ⅱ:采取逆推法,抓住碳链骨架的变化及官能团的变化及性质,并根据反应条件判断反应类型和相关物质.如转化关系中反应条件是KMnO4,我们就想到是氧化反应,再结合题干信息,便知是双键断裂;看到反应条件浓H2SO4,便猜测消去反应或酯化反应,再结合前后转化关系,得出正确结论.
解答:解:Ⅰ:D和A、B都能生成气体,而题给离子中只有H+与CO32-、OH-与NH4+能反应生成气体,故D只能为(NH4)2CO3;在A或D中滴入C,均有沉淀生成,说明A中含有SO42-,C中应含有Ba2+,而A和D反应生成的气体说明A一定是硫酸,产生的气体是二氧化碳,能被B吸收,说明B是一种碱,所以C是硝酸钡,B是氢氧化钠.
Ⅱ:结合题中有关信息聚丁烯酸甲酯结构简式用逆推法.由聚丁烯酸甲酯结构简式可知F应为CH3CH=CHCOOCH3,E是CH3CH=CHCOOH;由D→E的浓H2SO4条件可知这是一个醇的消去反应,D应该是羟基酸;再由题中二个方程式的信息及A的反应物不难推出A、B、C、D
在反应过程中,反应①③⑥中反应物全部转化为期望的产品,没有其它副产物,反应①③⑥符合题中的要求.
故答案为:
Ⅰ:A.H2SO4C.Ba(NO3)2
Ⅱ:(1)B: D:
D: (2)消去(或脱水) (3)①③⑥
(2)消去(或脱水) (3)①③⑥
Ⅱ:结合题中有关信息聚丁烯酸甲酯结构简式用逆推法.由聚丁烯酸甲酯结构简式可知F应为CH3CH=CHCOOCH3,E是CH3CH=CHCOOH;由D→E的浓H2SO4条件可知这是一个醇的消去反应,D应该是羟基酸;再由题中二个方程式的信息及A的反应物不难推出A、B、C、D
在反应过程中,反应①③⑥中反应物全部转化为期望的产品,没有其它副产物,反应①③⑥符合题中的要求.
故答案为:
Ⅰ:A.H2SO4C.Ba(NO3)2
Ⅱ:(1)B:
 D:
D: (2)消去(或脱水) (3)①③⑥
(2)消去(或脱水) (3)①③⑥点评:有机推断几乎是高考不变的一个题型,每年高考中必考,而给出某反应信息要求学生加以应用,能较好的考查考生的阅读、自学能力和思维能力,是热点题型.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目

