题目内容
常温下,有pH为12的NaOH溶液100 mL,若将其pH变为11(设溶液的体积可直接相加;计算结果保留到小数点后一位)。(1)若用pH=10的NaOH溶液,应加入____________mL。
(2)若用pH=2的盐酸,应加入____________mL。
(3)若用0.01 mol·L-1的CH3COOH溶液V1 mL,则V1的取值为____________。
(4)若用pH=2的任意一元酸HA溶液V2 mL,则V2的取值为____________。
(1)1000 (2)81.8 (3)V1>81.8 mL (4)0<V2≤81.8 mL
解析:(1)设加入pH=10的NaOH溶液体积为y。
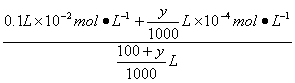 =0.001 mol·L-1
=0.001 mol·L-1
解得y=1000 mL
(2)设加入HCl溶液体积为V。
 =0.001 mol·L-1
=0.001 mol·L-1
解得V=81.8 mL
(3)CH3COOH是弱酸,要使pH由12降到11,则V(CH3COOH)>V(盐酸)=81.8 mL
(4)若HA为强酸,则V2=81.8 mL,若HA为弱酸,V2<81.8 mL。

| |||||||||||||||
| |||||||||||||||||||