题目内容
下列各组中的离子能大量共存于溶液中的是( )
| A、Na+、K+、HCO3-、OH- |
| B、Na+、H+、SiO32-、SO42- |
| C、K+、Cl-、NH4+、OH- |
| D、Na+、SiO32-、OH-、Cl- |
考点:离子共存问题
专题:离子反应专题
分析:离子能在溶液中大量共存,则离子之间不发生任何反应,如发生复分解反应生成沉淀、气体、弱电解质,或发生氧化还原反应、互促水解反应等.
解答:
解:A.OH-与HCO3-反应生成CO32-和水而不能大量共存,故A错误;
B.H+与SiO32-反应生成硅酸沉淀而不能大量共存,故B错误;
C.NH4+与OH-反应生成一水合氨而不能大量共存,故C错误;
D.离子之间不发生任何反应,可大量共存,故D正确.
故选D.
B.H+与SiO32-反应生成硅酸沉淀而不能大量共存,故B错误;
C.NH4+与OH-反应生成一水合氨而不能大量共存,故C错误;
D.离子之间不发生任何反应,可大量共存,故D正确.
故选D.
点评:本题考查离子共存问题,侧重于考查对元素化合物知识的综合应用能力,题目难度不大,注意把握离子的性质以及反应类型的判断,学习中注意积累.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
下列说法正确的是( )
| A、强电解质一定是离子化合物 |
| B、强酸、强碱及大部分盐类是强电解质 |
| C、强电解质的饱和溶液一定是浓溶液 |
| D、强电解质在水中一定能全部溶解 |
下列化合物中阳离子半径与阴离子半径比值最大的是( )
| A、NaF |
| B、LiI |
| C、MgI2 |
| D、KF |
下列说法不正确的是( )
| A、K+与Ar的结构示意图相同 |
B、二氧化碳的电子式: |
C、氧化钠的电子式: |
D、氯化氢的形成过程: |
下列有机物的命名正确的是( )
A、 2-乙基丙烷 2-乙基丙烷 |
| B、CH3CH2CHBrCH3 2-溴丁烷 |
C、 间二甲苯 间二甲苯 |
D、 2-甲基-2-丙烯 2-甲基-2-丙烯 |
对1mol/L的BaCl2溶液的有关叙述中,正确的是( )
| A、该溶液中Cl-浓度为0.5 mol/L |
| B、该溶液中Ba2+的物质的量是1 mol |
| C、该溶液中Ba2+和Cl-的物质的量之比为1:2 |
| D、将208g BaCl2固体溶解在1 L水中,所得溶液的浓度为1 mol/L |
近年来流行喝果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸( )是这种饮料的主要酸性物质.下列有关苹果酸性质的说法中,不正确的是( )
)是这种饮料的主要酸性物质.下列有关苹果酸性质的说法中,不正确的是( )
 )是这种饮料的主要酸性物质.下列有关苹果酸性质的说法中,不正确的是( )
)是这种饮料的主要酸性物质.下列有关苹果酸性质的说法中,不正确的是( )| A、可以与NaHCO3溶液反应产生CO2 |
| B、可以与乙醇发生酯化反应 |
| C、可以发生银镜反应 |
D、苹果酸与 互为同分异构体 互为同分异构体 |
下列物质中,按其成分与玻璃、水泥、陶瓷归于同一类的是( )
| A、石英 | B、碳化硅 |
| C、硅酸钠 | D、四氯化硅 |
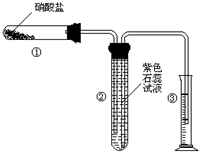 某校化学兴趣小组的同学对硝酸盐的受热分解进行探究.他们设计了如下装置分别加热了Ca(NO3)2、Cu(NO3)2、AgNO3三种固体.(加热及夹持装置未画出)
某校化学兴趣小组的同学对硝酸盐的受热分解进行探究.他们设计了如下装置分别加热了Ca(NO3)2、Cu(NO3)2、AgNO3三种固体.(加热及夹持装置未画出)