题目内容
在一定条件下,Na2CO3溶液存在水解平衡: CO32-+H2O HCO3-+OH-,下列说法正确的是( )
HCO3-+OH-,下列说法正确的是( )
 HCO3-+OH-,下列说法正确的是( )
HCO3-+OH-,下列说法正确的是( ) | A.稀释溶液,水解平衡常数增大 |
| B.加入NaOH固体,c(HCO3-)/c(CO32-) 减少 |
| C.升高温度,平衡常数减小 |
| D.通入CO2,pH增大 |
B
试题分析:稀释溶液,由于温度不变,水解平衡常数仍然不变,故A错误;加入NaOH固体,使得 CO32-+H2O
 HCO3-+OH-向左移动,所以c(HCO3-)/c(CO32-) 减少,故B正确,为本题的答案;水解过程是吸热过程,所以升高温度,平衡常数增大,故C错误;通入CO2,pH减小,所以D错误。
HCO3-+OH-向左移动,所以c(HCO3-)/c(CO32-) 减少,故B正确,为本题的答案;水解过程是吸热过程,所以升高温度,平衡常数增大,故C错误;通入CO2,pH减小,所以D错误。点评:本题考查了水解平衡,该考点是高考考查的热点,本题要注意水解过程是吸热过程,并且水解常数只于物质的性质和温度有关。

练习册系列答案
相关题目
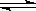 Ca2+ +2OH一中,能使c(Ca2+)减小,而使c(OH一)增大的是
Ca2+ +2OH一中,能使c(Ca2+)减小,而使c(OH一)增大的是
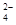 )的增大而减小
)的增大而减小