题目内容
(10分)某校化学兴趣小组采用酸碱中和滴定法测定学校新购入的烧碱的纯度(烧碱中含有不与酸反应的杂质),试根据实验回答。
(1)实验步骤为:①用托盘天平准确称量4.1g烧碱样品。
②将样品配 成250ml待测液,需要的仪器除玻璃棒、量筒、烧杯外还需要的玻璃仪器有______________________。
成250ml待测液,需要的仪器除玻璃棒、量筒、烧杯外还需要的玻璃仪器有______________________。
③用________、量取10.00ml待测 液,注入锥形瓶中。
液,注入锥形瓶中。
④在锥形瓶中滴入2~3滴________(填指示剂),用0.2010 mol/L的标准盐酸滴定待测烧碱溶液,滴定时左手旋转____式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视___________,直到滴定终点。
(2)实验过程中,下列操作将造成待测烧碱溶液浓度偏高的是_______________。
①量取待测液的滴定管没有用待测液润洗 ②锥形瓶水洗后又用待测液润洗
③未用标准盐酸溶液润洗滴定管 ④滴定过程中振荡时有液滴溅出
⑤滴定前盛装标准盐酸溶液的滴定管尖嘴部分无气泡,滴定后有气泡
⑥滴定前仰视读数,滴定后俯视读数
(3)该小组测得下列数据
| 滴定次数 | 待测液体积/ml | 标准盐酸体积/ml | |
| 滴定前读数/ml | 滴定后读数/ml | ||
| 第一次 | 10.00 | 0.20 | 22.90 |
| 第二次 | 10.00 | 0.50 | 20.40 |
| 第三次 | 10.00 | 4.00 | 24.10 |
| 第四次 | 10.00 | 0.00 | 20.00 |
(10分)(1) ②250ml容量瓶,胶头滴管。(2分) ③碱式滴定管。(1分)④酚酞或甲基橙,(1分)酸,(1分)锥形瓶内溶液颜色的变化,(1分)(2) ②③ (2分)(3)98%。(2分)
②③ (2分)(3)98%。(2分)
解析

 阅读快车系列答案
阅读快车系列答案(10分)某校化学兴趣小组采用酸碱中和滴定法测定学校新购入的烧碱的纯度(烧碱中含有不与酸反应的杂质),试根据实验回答。
(1)实验步骤为:①用托盘天平准确称量4.1g烧碱样品。
②将样品配成250ml待测液,需要的仪器除玻璃棒、量筒、烧杯外还需要的玻璃仪器有______________________。
③用________、量取10.00ml待测液,注入锥形瓶中。
④在锥形瓶中滴入2~3滴________(填指示剂),用0.2010mol/L的标准盐酸滴定待测烧碱溶液,滴定时左手旋转____式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视___________,直到滴定终点。
(2)实验过程中,下列操作将造成待测烧碱溶液浓度偏高的是_______________。
①量取待测液的滴定管没有用待测液润洗 ②锥形瓶水洗后又用待测液润洗
③未用标准盐酸溶液润洗滴定管 ④滴定过程中振荡时有液滴溅出
⑤滴定前盛装标准盐酸溶液的滴定管尖嘴部分无气泡,滴定后有气泡
⑥滴定前仰视读数,滴定后俯视读数
(3)该小组测得下列数据
| 滴定次数 | 待测液体积/ml | 标准盐酸体积/ml | |
| 滴定前读数/ml | 滴定后读数/ml | ||
| 第一次 | 10.00 | 0.20 | 22.90 |
| 第二次 | 10.00 | 0.50 | 20.40 |
| 第三次 | 10.00 | 4.00 | 24.10 |
| 第四次 | 10.00 | 0.00 | 20.00 |
根据上述数据,计算烧碱的纯度______________。
(15分)某校化学兴趣小组为了探究粗铁粒(含有少量金属铜杂质)与某浓度硝酸反应,设计了如下探究活动:
探究一
(1)将粗铁粒投入某浓度硝酸中,某同学观察该实验现象时发现,反应进行一段时间后,反应开始逐渐加快。请分析反应逐渐加快的可能原因
_______________________________________________________________________。
(2)另称取粗铁粒10 g放入某浓度硝酸中,充分反应后得到溶液X并收集到气体Y。为了探究溶液X中铁元素的价态,同学甲设计如下实验:有药品和仪器:0.1mol·L-1 KSCN溶液;0.1 mol·L-1 KI溶液;0.2 mol·L-1酸性高锰酸钾溶液;氯水等;试管和滴管
请你设计简单实验,探究上述猜想是否正确,填写下列实验报告:
| 实验步骤 | 现象 | 结论 | 离子方程式 |
| 第一步 | 取2-3 mL溶液装于试管,向试管中加入几滴KSCN溶液。 | | |
| 第二步 | | 若溶液紫色褪去,则溶液含有Fe2+; 若无明显变化,则不含Fe3+。 | |
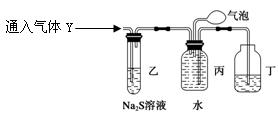
(3)装置乙的作用: 。
(4)装置丙收集到满气体后,通过气泡鼓入空气后,有红棕色气体生成,能否确定
气体Y中含NO?说明理由。
________________________________________________________________________。
(5) 同学丁为了探究气体Y的组成,将224mL气体Y通入足量的NaOH溶液中,气体被完全吸收,所得溶液再用0.15 mol·L-1酸性KMnO4溶液滴定,消耗20 mLKMnO4溶液。
则气体Y中NO、NO2的体积比为 。
(已知2NO2+2NaOH=NaNO3+NaNO2+H2O和NO2+NO+2NaOH=2NaNO2+H2O)
(10分)某校化学兴趣小组采用酸碱中和滴定法测定学校新购入的烧碱的纯度(烧碱中含有不与酸反应的杂质),试根据实验回答。
(1)实验步骤为:①用托盘天平准确称量4.1g烧碱样品。
②将样品配成250ml待测液,需要的仪器除玻璃棒、量筒、烧杯外还需要的玻璃仪器有______________________。
③用________、量取10.00ml待测液,注入锥形瓶中。
④在锥形瓶中滴入2~3滴________(填指示剂),用0.2010 mol/L的标准盐酸滴定待测烧碱溶液,滴定时左手旋转____式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视___________,直到滴定终点。
(2)实验过程中,下列操作将造成待测烧碱溶液浓度偏高的是_______________。
①量取待测液的滴定管没有用待测液润洗 ②锥形瓶水洗后又用待测液润洗
③未用标准盐酸溶液润洗滴定管 ④滴定过程中振荡时有液滴溅出
⑤滴定前盛装标准盐酸溶液的滴定管尖嘴部分无气泡,滴定后有气泡
⑥滴定前仰视读数,滴定后俯视读数
(3)该小组测得下列数据
|
滴定次数 |
待测液体积/ml |
标准盐酸体积/ml |
|
|
滴定前读数/ml |
滴定后读数/ml |
||
|
第一次 |
10.00 |
0.20 |
22.90 |
|
第二次 |
10.00 |
0.50 |
20.40 |
|
第三次 |
10.00 |
4.00 |
24.10 |
|
第四次 |
10.00 |
0.00 |
20.00 |
根据上述数据,计算烧碱的纯度______________。