题目内容
【题目】氢化钙(CaH2)固体是登山运动员常用的能源提供剂.氢化钙要密封保存,一旦接触到水就发生反应生成氢氧化钙和氢气,氢化钙在一定条件下与氧气反应生成的产物不只一种.氢化钙通常用氢气与金属钙加热制取,如图1是模拟制取装置. 
请回答下列问题:
(1)利用上述装置制取氢化钙时按气流方向连接顺序为(填仪器接口的字母编号).
i→→→→→→→a
(2)装有无水氯化钙装置的作用是 .
(3)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;打开分液漏斗活塞;(请按正确的顺序填入下列步骤的标号).
A.加热反应一段时间
B.收集气体并检验其纯度
C.关闭分液漏斗活塞
D.停止加热,充分冷却
(4)甲同学设计了一个实验,测定上述实验中得到的氢化钙的纯度.请完善下列实验步骤:
①样品称量;
②加入溶液(填化学式),搅拌;
③(填操作名称);洗涤;干燥
④称量碳酸钙.
(5)利用上述题目中给出的装置(试剂可另选)设计实验,用化学方法证明产物中含有氢化钙,写出实验简要步骤及观察到的现象 .
(6)乙同学利用图2所示装置测定上述实验中得到的氢化钙的纯度.他称取46mg所制得的氢化钙样品,记录开始时注射器活栓停留在lO.00mL刻度处,反应结束后充分冷却,活栓最终停留在57.04mL刻度处(上述气体体积均在标准状况下测定).试通过计算求样品中氢化钙的纯度: .
【答案】
(1)e;f;d;c;j(或k);k(或j)
(2)干燥氢气
(3)ABCD
(4)Na2CO3;过滤
(5)取适量氢化钙,在氧气中燃烧,用无水硫酸铜检验生成物,若固体变蓝,说明是氢化钙
(6)91.3%
【解析】解:(1)钙属于极活泼的金属,极易与水反应生成氢氧化钙和氢气,而制备的氢气中会混有水蒸气和氯化氢,所以在与钙化合之前需要除杂和干燥,分别选用试剂是氢氧化钠和浓硫酸;同时为防止空气中水蒸气进入,最后还需要连接干燥管,所以正确的顺序为:i→e→f→d→c→j(或k)→k(或j)→a;
所以答案是:i→e→f→d→c→j(或k)→k(或j)→a;(2)装有无水氯化钙装置的作用是干燥氢气,所以答案是:干燥氢气;(3)有气体参加加热或燃烧的反应需要首先验纯,实验完毕后先熄火、冷却,再停止气体生成,防止倒吸发生爆炸,故正确的操作顺序为:BADC,
所以答案是:BADC;(4)从最终称量碳酸钙可知,应加入碳酸钠溶液,使CaH2反应的同时得到碳酸钙沉淀,然后经过滤、洗涤、烘干、称量,确定纯度,
所以答案是:Na2CO3;过滤;(5)取适量氢化钙,在加热条件下与干燥氧气反应,将反应气相产物通过装有无水硫酸铜的干燥管,观察到白色变为蓝色证明为氢化钙,
所以答案是:取适量氢化钙,在氧气中燃烧,用无水硫酸铜检验生成物,若固体变蓝,说明是氢化钙;(6)由注射器D开始时活塞停留在10mL刻度处,反应结束后充分冷却,活塞最终停留57.04mL刻度处,可知生成氢气:57.04mL﹣10mL=47.04mL,所以氢气的质量为: ![]() ×2g/mol=0.0042g=4.2mg,设混合物中氢化钙的质量为x,生成氢气质量为y,则钙的质量为46mg﹣x,钙与水反应生成氢气质量为4.2mg﹣y,则:
×2g/mol=0.0042g=4.2mg,设混合物中氢化钙的质量为x,生成氢气质量为y,则钙的质量为46mg﹣x,钙与水反应生成氢气质量为4.2mg﹣y,则:
CaH2 | +2H2O═Ca(OH)2+ | 2H2↑ | ||
42 | 4 | |||
x | y |
所以42:4=x:y,
整理的y= ![]()
Ca | +2H2O═Ca(OH)2+ | H2↑ | ||
40 | 2 | |||
46mg﹣x | 4.2mg﹣y |
所以40:2=(46mg﹣x):(4.2mg﹣y),
将y= ![]() 代入,解得x=42mg,
代入,解得x=42mg,
所以样品中氢化钙的纯度为: ![]() ×100%=91.30%,
×100%=91.30%,
所以答案是:91.3%.

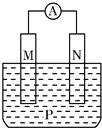
【题目】如图所示装置中,观察到电流计指针偏转;M棒变粗;N棒变细,由此判断表中所列M、N、P物质,其中可以成立的是( )
M | N | P | |
A | Zn | Cu | 稀H2SO4溶液 |
B | Cu | Fe | 稀HCl溶液 |
C | Ag | Zn | AgNO3溶液 |
D | Zn | Fe | Fe(NO3)3溶液 |
A.A
B.B
C.C
D.D
【题目】某同学进行下列实验:下列说法合理的是( )
装置 | 操作 | 现象 |
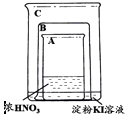
| 将盛有浓硝酸的烧杯A放入盛有淀粉KI溶液的烧杯C中,然后将铜片放入烧杯A后,立即用烧杯B罩住 | 烧杯A液体上方立即出现大量红棕色气体;一段时间后,红棕色气体消失,烧杯A和C中的液体都变成蓝色 |
A.烧杯A中发生反应:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O
B.红棕色气体消失只与NO2和烧杯C中的KI发生反应有关
C.烧杯C中溶液变蓝只与NO2和C中溶液发生反应有关
D.若将铜片换成铁片,则C中的液体也可能变蓝