题目内容
由SiO2、CuO、FeO、C中的某几种物质组成的混合粉末,取样品进行下列实验.
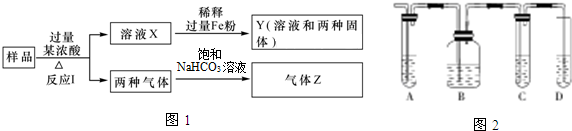
(1)由反应Ⅰ现象可知,该固体混合物中一定含有 (填化学式,下同),一定不含 .
(2)Z为一种或两种气体:
①若Z只为一种气体,为了验证反应I中的气体成分,设计了下列实验(如图2).A、B、C、D装置中可盛放的试剂是:
A ,B ,C ,D ,(填序号)
a.品红溶液 b.澄清石灰水 c.氢氧化钠溶液 d.KMnO4酸性溶液
②若Z为两种气体的混合物,则反应Ⅰ中的浓酸为 .
(3)向Y中通入过量氯气,并不断搅拌,充分反应后溶液中存在的阳离子是 (填离子符号).

(1)由反应Ⅰ现象可知,该固体混合物中一定含有
(2)Z为一种或两种气体:
①若Z只为一种气体,为了验证反应I中的气体成分,设计了下列实验(如图2).A、B、C、D装置中可盛放的试剂是:
A
a.品红溶液 b.澄清石灰水 c.氢氧化钠溶液 d.KMnO4酸性溶液
②若Z为两种气体的混合物,则反应Ⅰ中的浓酸为
(3)向Y中通入过量氯气,并不断搅拌,充分反应后溶液中存在的阳离子是
分析:(1)根据图1实验现象及生成物进行分析;
(2)①根据Z只为一种气体,说明浓酸为浓硫酸,气体Z为二氧化碳,按照检验二氧化碳中是否含有二氧化硫、除去杂质二氧化硫、再次检验、通过澄清石灰水检验二氧化碳的顺序选择试剂;
②若Z为两种气体的混合物,说明是浓硝酸与C反应生成了二氧化氮和二氧化碳;
(3)根据溶液X加入过量铁粉进行分析.
(2)①根据Z只为一种气体,说明浓酸为浓硫酸,气体Z为二氧化碳,按照检验二氧化碳中是否含有二氧化硫、除去杂质二氧化硫、再次检验、通过澄清石灰水检验二氧化碳的顺序选择试剂;
②若Z为两种气体的混合物,说明是浓硝酸与C反应生成了二氧化氮和二氧化碳;
(3)根据溶液X加入过量铁粉进行分析.
解答:解:(1)样品与浓酸能够生成两种气体和溶液,所以一定含有C,二氧化硅性质稳定,不溶于酸,一定没有二氧化硅,
故答案为:C;SiO2;
(2)①能够与碳反应浓酸为浓硫酸或者浓硝酸,生成的气体为二氧化硫或者二氧化氮,由于Z是一种气体,所以Z只能为二氧化碳,浓酸为浓硫酸,检验二氧化碳的方法为,先通过品红,检验气体中是否含有二氧化硫;然后通过高锰酸钾溶液,除去气体中可能混有的杂质二氧化硫,再次通过品红溶液检验气体中不含二氧化硫,最后通过澄清石灰水检验,所以A、B、C、D装置中可盛放的试剂分别为a、d、a、b,
故答案为:a;d;a;b;
②由于若Z为两种气体的混合物,浓酸只能是浓硝酸,浓硝酸与碳反应生成二氧化氮和二氧化碳,二氧化氮与饱和碳酸氢钠溶液反应生成一氧化氮,混合气体Z为一氧化氮和二氧化氮,
故答案为:浓硝酸;
(3)溶液X加入过量铁粉,得到的两种固体为置换出的铜和剩余的铁粉,溶液为亚铁离子的溶液,加入过量氯气后,溶液为氯水,含有次氯酸和氯化氢,溶液中铁粉、亚铁离子被氧化成铁离子、铜被被氧化成铜离子,溶液中含有氢离子,所以充分反应后溶液中存在的阳离子为Fe3+、Cu2+、H+,
故答案为:Fe3+、Cu2+、H+.
故答案为:C;SiO2;
(2)①能够与碳反应浓酸为浓硫酸或者浓硝酸,生成的气体为二氧化硫或者二氧化氮,由于Z是一种气体,所以Z只能为二氧化碳,浓酸为浓硫酸,检验二氧化碳的方法为,先通过品红,检验气体中是否含有二氧化硫;然后通过高锰酸钾溶液,除去气体中可能混有的杂质二氧化硫,再次通过品红溶液检验气体中不含二氧化硫,最后通过澄清石灰水检验,所以A、B、C、D装置中可盛放的试剂分别为a、d、a、b,
故答案为:a;d;a;b;
②由于若Z为两种气体的混合物,浓酸只能是浓硝酸,浓硝酸与碳反应生成二氧化氮和二氧化碳,二氧化氮与饱和碳酸氢钠溶液反应生成一氧化氮,混合气体Z为一氧化氮和二氧化氮,
故答案为:浓硝酸;
(3)溶液X加入过量铁粉,得到的两种固体为置换出的铜和剩余的铁粉,溶液为亚铁离子的溶液,加入过量氯气后,溶液为氯水,含有次氯酸和氯化氢,溶液中铁粉、亚铁离子被氧化成铁离子、铜被被氧化成铜离子,溶液中含有氢离子,所以充分反应后溶液中存在的阳离子为Fe3+、Cu2+、H+,
故答案为:Fe3+、Cu2+、H+.
点评:本题考查了几种未知物的检验,解题关键是合理分析题中信息,根据所学知识解答,充分考查了学生的分析、理解能力,本题难度中等.

练习册系列答案
相关题目




 某粉末试样由几种常见氧化物组成.向该粉末试样中加入过量的氢氧化钠溶液,充分溶解后过滤得红棕色固体和无色溶液,向所得无色溶液中滴入盐酸,产生沉淀的质量与所加盐酸的体积的关系如图所示,组成该粉末试样的氧化物可能是( )
某粉末试样由几种常见氧化物组成.向该粉末试样中加入过量的氢氧化钠溶液,充分溶解后过滤得红棕色固体和无色溶液,向所得无色溶液中滴入盐酸,产生沉淀的质量与所加盐酸的体积的关系如图所示,组成该粉末试样的氧化物可能是( )