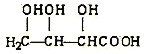题目内容
【题目】利用甲烷与氯气发生取代反应的副产品生产盐酸的设想在工业上已成为现实。某化学兴趣小组拟在实验室中模拟上述过程,所设计的装置如下图所示:
(1)A中制取C12反应的化学方程式是_____________________________。
(2)D装置中的石棉上吸附着潮湿的KI粉末,其作用是_________________________。
(3)E装置的作用是______________(填序号)。
A.收集气体B.吸收氯气C.吸收氯化氢
(4)E装置中除了有盐酸生成外,还含有有机物,从E中分离出盐酸的最佳方法是______________。
(5)将lmolCH4与C12发生取代,测得4种有机取代物的物质的量相等,则消耗的氯气的物质的量是______________。
【答案】 MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O 除去Cl2 C( 分液 2.5mol
MnCl2+Cl2↑+2H2O 除去Cl2 C( 分液 2.5mol
【解析】(1)MnO2能将HCl(浓)氧化为MnCl2和Cl2,A中制取Cl2反应的化学方程式MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)湿润的KI粉末可以用来除去过量的氯气,发生反应:2KI+Cl2=2KCl+I2;
(3)由于上述过程中产生的氯气和HCl均易导致大气污染,所以E的作用是吸收尾气,HCl极易溶于水易发生倒吸,所以E还可以防止倒吸,故答案为C;
(4)E装置中除了有盐酸生成外,还含有二氯甲烷、三氯甲烷和四氯化碳,二氯甲烷、三氯甲烷和四氯化碳不溶于水,能分层,可用分液分开;
(5)1mol甲烷完全与氯气发生取代反应,若生成相同物质的量的四种取代物,所以每种取代物的物质的量是0.25mol,甲烷和氯气的取代反应中,被取代的氢原子的物质的量与氯气的物质的量相等,所以生成0.25mol一氯甲烷需要氯气0.25mol氯气,生成0.25mol二氯甲烷需要氯气0.5mol,生成0.25mol三氯甲烷需要氯气0.75mol氯气,生成0.25mol四氯化碳需要氯气1mol,所以总共消耗氯气的物质的量=0.25mol+0.5mol+0.75mol+1mol=2.5mol。

【题目】有机物X(分子式为C4H6O5)广泛存在于许多水果中,尤以苹果、葡萄、西瓜、山楂内为多。经测定该有机物具有下列性质(见下表)。请根据题目要求填空:
X的性质 | |
① | X与足量的金属钠反应产生氢气 |
② | X与醇或羧酸在浓硫酸加热条件下均能生成有香味的产物 |
③ | 在一定条件下X的分子内脱水产物(不是环状化合物)可与溴水发生加成反应 |
④ | 33.5gX与100mL的5mol/LNaOH溶液恰好完全中和 |
(1)X的可能结构简式I:________,Ⅱ:__________,Ⅲ:__________。
(2)在一定条件下有机物X可发生化学反应的类型有(填序号)__________。
A.水解反应 B.取代反应 C.加成反应 D.消去反应 E.加聚反应 F.中和反应
(3)下列物质与X互为同系物的是(填序号)_______,与X互为同分异构体的是(填序号)_______。
(a)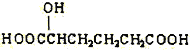 (b)
(b)![]()
(c)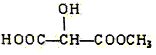 (d)H3COOC-COOCH3
(d)H3COOC-COOCH3
(e)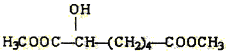 (f)
(f)