题目内容
在某稀硝酸的溶液中,加入5.6g铁粉充分反应后,铁粉全部溶解,放出NO气体,溶液质量增加3.2g,所得溶液中Fe2+和Fe3+物质的量之比为( )A.1:1
B.2:1
C.3:2
D.4:1
【答案】分析:由信息可知铁与硝酸反应生成Fe2+和Fe3+,反应掉铁的质量与生成NO的质量之差为3.2g,利用质量关系和电子守恒来计算.
解答:解:n(Fe)=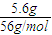 =0.1mol,生成NO的质量为5.6g-3.2g=2.4g,n(NO)=
=0.1mol,生成NO的质量为5.6g-3.2g=2.4g,n(NO)=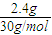 =0.08mol,
=0.08mol,
设Fe2+和Fe3+物质的量分别为x、y,则
 ,
,
解得x=0.06mol,y=0.04mol,
所以所得溶液中Fe2+和Fe3+物质的量之比为0.06mol:0.04mol=3:2,
故选C.
点评:本题考查铁与硝酸反应的计算,明确NO的质量及原子守恒、电子守恒是解答本题的关键,难度不大.
解答:解:n(Fe)=
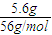 =0.1mol,生成NO的质量为5.6g-3.2g=2.4g,n(NO)=
=0.1mol,生成NO的质量为5.6g-3.2g=2.4g,n(NO)=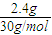 =0.08mol,
=0.08mol,设Fe2+和Fe3+物质的量分别为x、y,则
 ,
,解得x=0.06mol,y=0.04mol,
所以所得溶液中Fe2+和Fe3+物质的量之比为0.06mol:0.04mol=3:2,
故选C.
点评:本题考查铁与硝酸反应的计算,明确NO的质量及原子守恒、电子守恒是解答本题的关键,难度不大.

练习册系列答案
相关题目