题目内容
(15)钢铁工业是国家工 业的基础,请回答钢铁腐蚀与防护过程中的有关问题。
业的基础,请回答钢铁腐蚀与防护过程中的有关问题。
(1)生产中可用盐酸来除铁锈。现将一生锈的铁片 放入
放入 盐酸中,当铁锈被除尽后,溶液中发生的化合反应的化学方程式
盐酸中,当铁锈被除尽后,溶液中发生的化合反应的化学方程式
________________________________________________________________________。
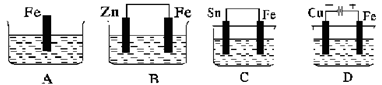
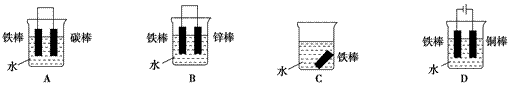
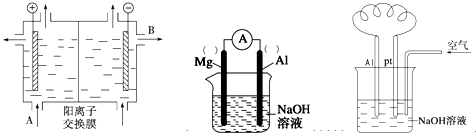
(2)下列哪个装置可防止铁棒被腐蚀__________________________________(填编号)。
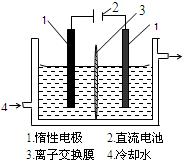
(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图:
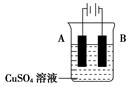
①A电极对应的金属是________(写元素名称),B电极的电极反应式是________。
②若电镀前A、B两金属片质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12 g,则电镀时电路中通过的电子为________mol。
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原 因
因
________________________________________________________________________。
 业的基础,请回答钢铁腐蚀与防护过程中的有关问题。
业的基础,请回答钢铁腐蚀与防护过程中的有关问题。(1)生产中可用盐酸来除铁锈。现将一生锈的铁片
 放入
放入 盐酸中,当铁锈被除尽后,溶液中发生的化合反应的化学方程式
盐酸中,当铁锈被除尽后,溶液中发生的化合反应的化学方程式________________________________________________________________________。
(2)下列哪个装置可防止铁棒被腐蚀__________________________________(填编号)。

(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图:

①A电极对应的金属是________(写元素名称),B电极的电极反应式是________。
②若电镀前A、B两金属片质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12 g,则电镀时电路中通过的电子为________mol。
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原
 因
因________________________________________________________________________。
(15分)(1)2FeCl3+Fe===3FeCl2 (2) BD
(3)① 铜 Cu2++2e-―→Cu ② 0.08 ③ 铁比铜活泼,镀层破坏后,在潮湿环境中形成原电池,铁为负极,加速铁的腐蚀(答案叙述合理即可)
(3)① 铜 Cu2++2e-―→Cu ② 0.08 ③ 铁比铜活泼,镀层破坏后,在潮湿环境中形成原电池,铁为负极,加速铁的腐蚀(答案叙述合理即可)
略

练习册系列答案
相关题目
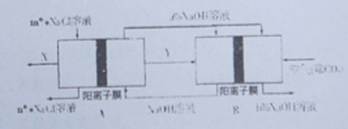
 水的产物),试用有关的电极反应式,离子方程式和化学方程式表示Fe(OH)3的生成:
水的产物),试用有关的电极反应式,离子方程式和化学方程式表示Fe(OH)3的生成: ;
;

 B____________________
B____________________