题目内容
填空题(1)将复杂硅酸盐改写成氧化物形式:KAlSi3O8:
(2)有一包白色粉末可能由K2SO4、NaHCO3、BaCl2、FeCl3、KCl五种物质中的某几种组成,现进行如下实验:
①将白色粉末加水溶解,得无色溶液.
②向①中所得的无色溶液中加入NaOH溶液,观察到有白色沉淀A生成,过滤后,向滤液中滴加硝酸酸化的AgNO3溶液,又得到白色沉淀B.
根据上述现象判断:
①A的化学式是
②原白色粉末中一定含有
A.①②③④B.④①②③C.④②①②③④D.①③②④
分析:(1)根据硅酸盐化学式可表示为活泼金属氧化物?金属氧化物?非金属氧化物?水进行解答;
(2)无色溶液中,有色离子不能存在无FeCl3;能和氢氧化钠反应并产生白色沉淀的是碳酸氢钠以及氯化钡溶液,氯化钡溶液中含有氯离子,能和硝酸酸化的硝酸银之间反应生成氯化银白色沉淀;原溶液一定不含有硫酸钾,可能含氯化钾,根据焰色反应操作进行解答;
(2)无色溶液中,有色离子不能存在无FeCl3;能和氢氧化钠反应并产生白色沉淀的是碳酸氢钠以及氯化钡溶液,氯化钡溶液中含有氯离子,能和硝酸酸化的硝酸银之间反应生成氯化银白色沉淀;原溶液一定不含有硫酸钾,可能含氯化钾,根据焰色反应操作进行解答;
解答:解:(1)硅酸盐由盐的书写改写为氧化物的形式即改写的一般方法归纳为:碱性氧化物、两性氧化物、酸性氧化物、水(xMO?nSiO2?mH2O),所以KAlSi3O8可表示为:K2O?Al2O3?6SiO2,
故答案为:K2O?Al2O3?6SiO2;
(2)①FeCl3溶液为棕黄色,将白色粉末加水溶解,得无色溶液,所以一定不含有FeCl3,向①中中所得的无色溶液中加入NaOH溶液并加热,仅观察到有白色沉淀A生成,则一定含有碳酸氢钠和氯化钡,碳酸氢钠可以和氢氧化钠反应得到碳酸钠,碳酸钠可以和氯化钡反应生成碳酸钡白色沉淀,过滤后,向滤液中滴加硝酸酸化的AgNO3溶液,又得到白色沉淀B,即为氯化银沉淀,故答案为:BaCO3;AgCl;
有白色沉淀A生成,则一定含有碳酸氢钠和氯化钡,有氯化钡就一定没有硫酸钾,白色沉淀B为氯化银沉淀,氯离子可能是氯化钡中的氯离子,不能确定是否含有KCl,钾离子的检验,可通过焰色反应检验,焰色反应的操作步骤:④用稀盐酸洗净铂丝,②置酒精灯火焰上灼烧,①蘸取待测液,②置于酒精灯火焰上灼烧,③透过蓝色钴玻璃观察火焰颜色,④用稀盐酸洗净铂丝,故C符合,
②故答案为:NaHCO3、BaCl2;KCl;焰色;C;
故答案为:K2O?Al2O3?6SiO2;
(2)①FeCl3溶液为棕黄色,将白色粉末加水溶解,得无色溶液,所以一定不含有FeCl3,向①中中所得的无色溶液中加入NaOH溶液并加热,仅观察到有白色沉淀A生成,则一定含有碳酸氢钠和氯化钡,碳酸氢钠可以和氢氧化钠反应得到碳酸钠,碳酸钠可以和氯化钡反应生成碳酸钡白色沉淀,过滤后,向滤液中滴加硝酸酸化的AgNO3溶液,又得到白色沉淀B,即为氯化银沉淀,故答案为:BaCO3;AgCl;
有白色沉淀A生成,则一定含有碳酸氢钠和氯化钡,有氯化钡就一定没有硫酸钾,白色沉淀B为氯化银沉淀,氯离子可能是氯化钡中的氯离子,不能确定是否含有KCl,钾离子的检验,可通过焰色反应检验,焰色反应的操作步骤:④用稀盐酸洗净铂丝,②置酒精灯火焰上灼烧,①蘸取待测液,②置于酒精灯火焰上灼烧,③透过蓝色钴玻璃观察火焰颜色,④用稀盐酸洗净铂丝,故C符合,
②故答案为:NaHCO3、BaCl2;KCl;焰色;C;
点评:本题考查硅酸盐改写为氧化物的形式的方法、溶液中溶质的成分分析,题目难度中等,注意硅酸盐改写为氧化物的一般方法为:碱性氧化物、两性氧化物、酸性氧化物、水(xMO?nSiO2?mH2O).解答本题要从物质的颜色、物质之间相互作用时的实验现象等方面进行分析、判断,从而得出正确的结论.

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目
(14分)(1)将复杂硅酸盐改写成氧化物形式:KAlSi3O8:________________
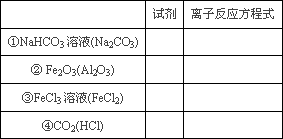
(2)除杂(括号内为杂质):请把所加试剂和有关离子反应方程式填在空白处。
| | 试剂 | 离子反应方程式 |
| ①NaHCO3溶液(Na2CO3) | | |
| ② Fe2O3(Al2O3) | | |
| ③FeCl3溶液(FeCl2) | | |
| ④CO2(HCl) | | |
(14分)(1)将复杂硅酸盐改写成氧化物形式:KAlSi3O8:________________
(2)除杂(括号内为杂质):请把所加试剂和有关离子反应方程式填在空白处。
|
|
试剂 |
离子反应方程式 |
|
①NaHCO3溶液(Na2CO3) |
|
|
|
② Fe2O3(Al2O3) |
|
|
|
③FeCl3溶液(FeCl2) |
|
|
|
④CO2(HCl) |
|
|