题目内容
10.1体积乙烯与足量氯气发生加成反应,该加成产物与足量氯气发生完全取代(反应在同温同压的条件下进行),则整个过程至少消耗氯气( )| A. | 3体积 | B. | 4体积 | C. | 5体积 | D. | 6体积 |
分析 依次发生反应:C2H4+Cl2→CH2ClCH2Cl,CH2ClCH2Cl+4Cl2$\stackrel{光照}{→}$CCl3CCl3+4HCl,结合方程式计算.
解答 解:由C2H4+Cl2→CH2ClCH2Cl,可知1mol乙烯与氯气发生加成反应需要氯气1mol,生成1molCH2ClCH2Cl,由CH2ClCH2Cl+4Cl2$\stackrel{光照}{→}$CCl3CCl3+4HCl,所以1molCH2ClCH2Cl与氯气发生取代反应,最多需要4mol氯气,故1mol乙烯转化为CCl3CCl3需要氯气为1mol+4mol=5mol,及1体积乙烯需要至少消耗5体积氯气,
故选:C.
点评 本题考查化学方程式计算,涉及加成反应、取代反应,明确化学反应中的量的关系即可解答,难度不大.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
20.下列高分子化合物所对应的结构单元正确的是( )
| A. | 聚氯乙烯 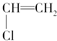 | B. | 聚苯乙烯 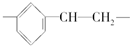 | ||
| C. | 聚异戊二烯  | D. | 聚丙烯-CH2-CH2-CH2- |
1.有一瓶澄清的溶液,其中可能含有NH4+、K+、Mg2+、Ba2+、Al3+、Fe3+、AlO2-、SO42-、CO32-、NO3-、Cl-中的几种,取该溶液进行以下实验.
(1)填表(填写离子符号或“无”)
(2)根据以上事实,该溶液中肯定存在的离子是NH4+、Ba2+、NO3-、Cl-.
(3)请设计实验方案检验未确定的其他离子是否存在:用洁净的铂丝蘸取原溶液进行焰色反应实验,通过蓝色钴玻璃观察,若看到火焰呈紫色,则原溶液中含有K+,反之则无.
(4)写出实验③、④中发生反应的离子方程式:
实验③Ba2++CO32-=BaCO3↓;
实验④NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
(1)填表(填写离子符号或“无”)
| 序号 | 实验步骤 | 肯定不存在的离子 |
| ① | 用pH试纸测得该溶液呈酸性 | |
| ② | 另取10mL该溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐变为碱性,在整个滴加过程中无沉淀生成 | |
| ③ | 往②所得溶液中加入足量Na2CO3溶液,过滤、洗涤、干燥,得到1.97g白色固体 | |
| ④ | 另取10mL该溶液,加入浓NaOH溶液并加热,收集到224mL,气体(标准状况) | |
| ⑤ | 另取10mL该溶液,加入足量稀HNO3和AgNO3,产生2.87g白色沉淀 |
(3)请设计实验方案检验未确定的其他离子是否存在:用洁净的铂丝蘸取原溶液进行焰色反应实验,通过蓝色钴玻璃观察,若看到火焰呈紫色,则原溶液中含有K+,反之则无.
(4)写出实验③、④中发生反应的离子方程式:
实验③Ba2++CO32-=BaCO3↓;
实验④NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
18.依据下表所列实验及现象得出的结论不正确的是( )
| 实验项目 | 实验现象 |
| FeCl3溶液中加入维生素C | 溶液褪色为浅绿色 |
| 饱和FeCl3溶液滴入沸水中 | 得到红褐色液体 |
| 将铜锈放入盐酸中 | 有无色气泡产生 |
| A. | 维生素C具有还原性 | B. | FeCl3水解生成Fe(OH)3胶体 | ||
| C. | 铜锈与盐酸反应有H2生成 | D. | 铜锈中含有碳酸根 |
2.为了除去氯化钠溶液中少量的溴化钠,常用的方法是往溶液中加入少量的氯水,然后加入苯或四氯化碳,经振荡、静置、分液,将氯化钠溶液加热排除溶解在水中的氯分子,得到氯化钠溶液.分析判断,正确的是( )
| A. | 加入苯或四氯化碳操作叫萃取 | B. | 苯层在下层或四氯化碳在上层 | ||
| C. | 可以用酒精代替苯或四氯化碳 | D. | 氯水是还原剂 |
19.下列离子方程式正确的是( )
| A. | 稀硫酸与氢氧化钡溶液反应:H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| B. | 硫酸铝溶液中滴入氨水:Al3++3OH-=Al(OH)3↓ | |
| C. | 铜粉加入FeCl3溶液:Cu+Fe3+=Cu2++Fe2+ | |
| D. | 硝酸铝溶液中滴加少量的氢氧化钠溶液:Al3++3OH-=Al(OH)3↓ |
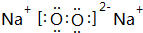 ,其化学键的类型为离子键、共价键.
,其化学键的类型为离子键、共价键.