��Ŀ����
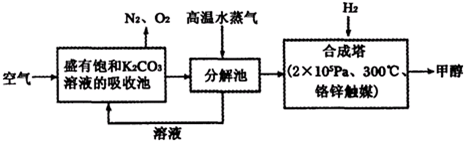
����̼���á����Ե��ܺġ�����Ⱦ�����ŷ�Ϊ�����Ŀɳ�����չ����ģʽ������˵���롰��̼���á������ϵ��ǣ�������
����������̼���á����Ե��ܺġ�����Ⱦ�����ŷ�Ϊ�����ľ���ģʽ����̼���þ���ָ���ƶ�����̼���ŷ������ݴ˼��ɽ��
����⣺A���л��ܼ�ָ��̼�Ļ������ˮ��Ⱦ�����з������л��ܼ����ˮ�롰��̼���á������ϣ���Aѡ��
B����ǿ��ú��ʯ�͡���Ȼ�����ۺ����õ��о������ȼ�ϵ������ʣ��ɼ��ٻ�ʯȼ�ϵ�ʹ�ã����ϡ���̼���á�ģʽ����B��ѡ��
C������CO2�ϳɾ�̼������ɽ������ϣ�ʵ�֡�̼����ѭ�����ã��ܼ��ٶ�����̼���ŷţ����ϡ���̼���á�����C��ѡ��
D������̫���ܵ�����Դ���ɼ���ʹ�û�ʯȼ���ŷ�����Դ�������Ⱦ��Ҳ���Լ��ٶ�����̼���ŷţ����ϡ���̼���á�����D��ѡ��
��ѡA��
B����ǿ��ú��ʯ�͡���Ȼ�����ۺ����õ��о������ȼ�ϵ������ʣ��ɼ��ٻ�ʯȼ�ϵ�ʹ�ã����ϡ���̼���á�ģʽ����B��ѡ��
C������CO2�ϳɾ�̼������ɽ������ϣ�ʵ�֡�̼����ѭ�����ã��ܼ��ٶ�����̼���ŷţ����ϡ���̼���á�����C��ѡ��
D������̫���ܵ�����Դ���ɼ���ʹ�û�ʯȼ���ŷ�����Դ�������Ⱦ��Ҳ���Լ��ٶ�����̼���ŷţ����ϡ���̼���á�����D��ѡ��
��ѡA��
���������⿼���ˡ���̼���á�����ע����ȵ㣬����鱾�����յ�֪ʶ�ǽ��Ĺؼ����ѶȲ���

��ϰ��ϵ�д�
 Сѧ���AB��ϵ�д�
Сѧ���AB��ϵ�д� ABC����ȫ�ž�ϵ�д�
ABC����ȫ�ž�ϵ�д�
�����Ŀ