题目内容
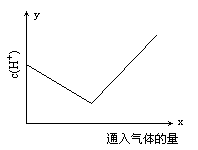
下图中横轴表示通入气体的量,纵轴表示溶液中H+的物质的量浓度。下列反应与下图中变化关系相符合的是( )
A.向饱和H2S溶液中通入过量的Cl2 B.向饱和H2S溶液中通入过量的SO2
C.向SO2饱和溶液中通入过量的H2S D.向浓H2SO4溶液中通入过量的SO2
解析:图象说明c(H+)随通入气体量的增大先减小后增大,反应前c(H+)比反应后c(H+)要小。
A项中,H2S是很弱的酸,溶液中c(H+)小,通入Cl2后发生反应为H2S+Cl2 ![]() 2HCl+S↓,生成的HCl完全电离,c(H+)不断增大,所以A项反应与图象不符合。
2HCl+S↓,生成的HCl完全电离,c(H+)不断增大,所以A项反应与图象不符合。
B项中,向饱和H2S溶液中通入SO2发生的反应为SO2+2H2S ![]() 2H2O+3S↓,随着SO2与H2S反应的进行,c(H+)逐渐减小,当H2S与SO2完全反应后,还继续通SO2,就形成亚硫酸,亚硫酸电离出H+,由于H2SO3的酸性强于H2S,最终c(H+)比反应前要大,所以符合图象关系。
2H2O+3S↓,随着SO2与H2S反应的进行,c(H+)逐渐减小,当H2S与SO2完全反应后,还继续通SO2,就形成亚硫酸,亚硫酸电离出H+,由于H2SO3的酸性强于H2S,最终c(H+)比反应前要大,所以符合图象关系。
C项中,反应开始c(H+)减小,H2SO3+2H2S ![]() 3S↓+3H2O。H2SO3反应完全,再通入H2S,当达饱和时,氢硫酸溶液中c(H+)要比原来小(H2SO3酸性比H2S强),所以不符合图象关系。
3S↓+3H2O。H2SO3反应完全,再通入H2S,当达饱和时,氢硫酸溶液中c(H+)要比原来小(H2SO3酸性比H2S强),所以不符合图象关系。
D项中,浓H2SO4不能氧化SO2,溶液中的H+浓度不会发生变化,与图象不符。
答案:B

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目