题目内容
如图实验装置用于验证某些物质的性质.在试管A中装入足量的固体NaHCO3.试回答下列问题:
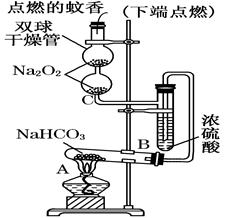
(1)在A试管内发生反应的化学方程式是_______________________________________________;
(2)B装置的作用是__________________________________________________;
(3)在双球干燥管内发生反应的化学方程式为___________________________________________;
(4)双球干燥管内观察到的实验现象是___ _____, 上述实验现象说明_________________ _;
(5)若将干燥管内的Na2O2换成Na2O,则双球干燥管内观察到的实验现象是______________________。

(1)在A试管内发生反应的化学方程式是_______________________________________________;
(2)B装置的作用是__________________________________________________;
(3)在双球干燥管内发生反应的化学方程式为___________________________________________;
(4)双球干燥管内观察到的实验现象是___ _____, 上述实验现象说明_________________ _;
(5)若将干燥管内的Na2O2换成Na2O,则双球干燥管内观察到的实验现象是______________________。
(1)2NaHCO3 Na2CO3+H2O+CO2↑ (1分)
Na2CO3+H2O+CO2↑ (1分)
(2)吸收气体中的水蒸气(干燥CO2)(1分)(3)2Na2O2+2CO2=2Na2CO3+O2(1分)
(4)淡黄色的Na2O2逐渐转变为白色粉末,点燃的蚊香燃烧更加剧烈(2分)
Na2O2能与CO2反应,生成白色粉末状物质和O2(2分) (5)点燃的蚊香逐渐熄灭(2分)
 Na2CO3+H2O+CO2↑ (1分)
Na2CO3+H2O+CO2↑ (1分)(2)吸收气体中的水蒸气(干燥CO2)(1分)(3)2Na2O2+2CO2=2Na2CO3+O2(1分)
(4)淡黄色的Na2O2逐渐转变为白色粉末,点燃的蚊香燃烧更加剧烈(2分)
Na2O2能与CO2反应,生成白色粉末状物质和O2(2分) (5)点燃的蚊香逐渐熄灭(2分)
试题分析:(1)碳酸氢钠不稳定,受热易分解,反应的化学方程式为2NaHCO3
 Na2CO3+H2O+CO2↑。
Na2CO3+H2O+CO2↑。(2)由于生成的CO2气体中含有水蒸气,所以浓硫酸的作用是吸收水蒸气,干燥CO2。
(3)CO2能和过氧化钠反应生成碳酸钠和氧气,反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2。
(4)CO2能和过氧化钠反应生成碳酸钠和氧气,所以实验现象是淡黄色的Na2O2逐渐转变为白色粉末,点燃的蚊香燃烧更加剧烈。
(5)由于氧化钠与CO2反应生成的是碳酸钠,得不到氧气,因此点燃的蚊香逐渐熄灭。

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目