题目内容
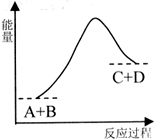 已知反应A+B=C+D的能量变化如图所示,下列说法正确的是( )
已知反应A+B=C+D的能量变化如图所示,下列说法正确的是( )| A、该反应是放热反应 | B、只有在加热条件下才能进行 | C、反应物的总能量高于生成物的总能量 | D、反应中断开化学键吸收的总能量高于形成化学键放出的总能量 |
分析:A、依据图象分析反应物能量低于生成物,结合能量守恒分析判断反应能量变化;
B、某些吸热反应不需要加热也可以发生;
C、图象分析可知反应过程中反应物能量低于生成物;
D、反应是吸热反应,依据反应实质分析,断裂化学键吸收能量,形成化学键放出能量;
B、某些吸热反应不需要加热也可以发生;
C、图象分析可知反应过程中反应物能量低于生成物;
D、反应是吸热反应,依据反应实质分析,断裂化学键吸收能量,形成化学键放出能量;
解答:解:A、图象分析反应物能量低于生成物,结合能量守恒分析反应是吸热反应,故A错误;
B、某些吸热反应不需要加热也可以发生,如氢氧化钡晶体和铵盐发生的吸热反应,故B错误;
C、图象分析可知反应过程中反应物能量低于生成物能量,故C错误;
D、反应是吸热反应,依据反应实质分析,断裂化学键吸收能量,形成化学键放出能量,反应中断开化学键吸收的总能量高于形成化学键放出的总能量,故D正确;
故选D.
B、某些吸热反应不需要加热也可以发生,如氢氧化钡晶体和铵盐发生的吸热反应,故B错误;
C、图象分析可知反应过程中反应物能量低于生成物能量,故C错误;
D、反应是吸热反应,依据反应实质分析,断裂化学键吸收能量,形成化学键放出能量,反应中断开化学键吸收的总能量高于形成化学键放出的总能量,故D正确;
故选D.
点评:本题考查了化学反应能量变化分析,图象分析方法和应用,注意反应吸热放热和反应条件关系的判断应用,题目较简单.

练习册系列答案
相关题目
已知反应A+B=C+D是放热反应,对该反应的下列说法正确的是( )
| A、该反应一定属于复分解反应 | B、A的能量一定大于C | C、A和B的总能量之和一定大于C和D的总能量之和 | D、反应过程中只有化学键的形成,没有化学键的断裂 |
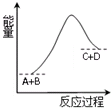 已知反应A+B=C+D的能量变化如图所示,下列说法正确的是( )
已知反应A+B=C+D的能量变化如图所示,下列说法正确的是( )| A、该反应为吸热反应 | B、A物质能量一定低于C物质能量 | C、该反应只有在加热条件下才能进行 | D、反应物的总能量高于生成物的总能量 |
 C+D为放热反应,对于该反应,下列说法中正确的是( )
C+D为放热反应,对于该反应,下列说法中正确的是( )