��Ŀ����
����Ŀ��ij��ȤС�����Ʊ���������֤��һϵ�����ʣ�ʵ��װ����ͼ��ʾ��ʡ�Լг�װ�ã�����֪����������ƣ�Na2S2O3����Һ�ڹ�ҵ�Ͽ���Ϊ���ȼ�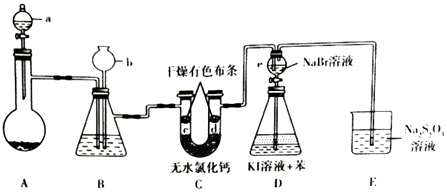
�ش��������⣺
��1������a�������� �� ����ʢ��Ũ���ᣬ��ƿA ��ʢ�еĹ����Լ������ѧʽ����
��2��װ��B��ʢ�б���NaCl��Һ��װ��B�������� ��
a����ȥC12�е�����HCl b������ c���ṩ����ˮ���� d���۲�װ���Ƿ����
��3��c����ɫ������ɫ����d������ɫ����˵�� ��
��4��ʵ�������e �Ļ�����ʹ���е���Һ���˵���ƿD�У�ҡ����ƿ�����ú�ɹ۲쵽
��5��װ��E�з�����Ӧ�����ӷ���ʽΪ ��
���𰸡�
��1����Һ©����KMnO4����KClO3���ȣ�
��2��acd
��3��Cl2��Ư�����ã�HClO��Ư������
��4���ϲ���ҺΪ�Ϻ�ɫ
��5��S2O32��+4Cl2+5H2O=2SO42��+8Cl��+10H+
���������⣺��1������a���в���������©����Ϊ��Һ©��������ʢ��Ũ���ᣬ��ƿA ���ڳ����������Ȼ�����ȡ��������ѡ��KMnO4����KClO3���ȣ�����ӦΪ��2KMnO4+16HCl�T2KCl+2MnCl2+5Cl2��+8H2O��KClO3+6HCl��Ũ��=KCl+3Cl2��+3H2O��
���Դ��ǣ���Һ©����KMnO4����KClO3���ȣ�����2�����������ڱ���ʳ��ˮ����HCl��������ˮ�����ñ���ʳ��ˮ��ȥ�������������Ȼ������壬����ͨ��C���������ɫ������������״��������ɹ۲쵽c��������ɫ��d������ɫ��װ��B�ṩ����ˮ��������������ʱB�еģ�ѹǿ����B�г���©����Һ���������γ�ˮ�����ɹ۲�װ���Ƿ����������acd���ϣ�
���Դ��ǣ�acd����3����װ��c��ͨ��������d������ɫ��������ɫ����Ϊ������������߱�Ư���ԣ�c������ɫ������ɫ����˵������������ҺB�������ˮ����ʪ����������Ư���ԣ�������Ư�����õ���������ˮ��Ӧ���ɵĴ��������Ư���ԣ�
���Դ��ǣ�Cl2��Ư�����ã�HC1O��Ư�����ã���4��ʵ�������e �Ļ�����ʹ���е���Һ���˵���ƿD�У���ˮ�м��뱽��ʳȺ췢����ȡ�������ܶȱ�ˮС���ϲ���ҺΪ�Ϻ�ɫ��
���Դ��ǣ��ϲ���ҺΪ�Ϻ�ɫ����5��Na2S2O3������+2�ۣ�����������SO42�� �� ��װ��E����Ӧ�����ӷ�Ӧ����ʽ��S2O32��+4Cl2+5H2O=2SO42��+8Cl��+10H+ ��
���Դ��ǣ�S2O32��+4Cl2+5H2O=2SO42��+8Cl��+10H+ ��

 ÿ�α���ϵ�д�
ÿ�α���ϵ�д�����Ŀ����A��B��C��D���ֽ������±���װ�ý���ʵ�顣
װ�� |
|
|
|
���� | ���۽���A�����ܽ� | C���������� | A����������� |
����ʵ������ش��������⣺
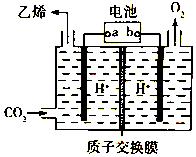
��1��װ�ü��и����ĵ缫��Ӧʽ��______________________________________��
��2��װ�����������ĵ缫��Ӧʽ��_______________________________________��
��3��װ�ñ�����Һ��pH________�����������������С����������������
��4�����ֽ��������ǿ������˳����___________________________________��