题目内容
( 13分)下表是元素周期表的一部分,请回答有关问题:(用元素符号)
|
|
IA |
ⅡA |
|
ⅢA |
ⅣA |
VA |
ⅥA |
ⅦA |
0 |
|
|
1 |
a |
|
b |
|||||||
|
2 |
|
|
|
|
c |
d |
e |
f |
g |
|
|
3 |
h |
|
i |
j |
|
|
k |
l |
||
|
4 |
m |
|
|
|
|
|
n |
|
||
(1)a元素与e元素形成的原子个数比为1:1的化合物的结构为式:_____________;
(2)n元素与f元素两者核电荷数之差是_____________________;
(3)上表中,原子半径最大的是(稀有气体除外)________________;
(4)推测j、d最简单氢化物的稳定性强弱关系____________(填化学式)。
(5)c2a4与n的单质反应的化学方程式______________________________;
(6)写出c5a12的所有同分异构体的结构简式_________________________。
(1)H—O—O—H (2)26 (3)K (4)NH3 > SiH4
(5)CH2=CH2+Br2 →CH2BrCH2Br
(6)CH3CH2CH2CH2CH3 CH3CH2CH(CH3)2 C(CH3)4 (3分)
【解析】(1)a元素与e元素分别是H和O,二者原子个数比为1:1的化合物是H2O2,结构式为H—O—O—H。
(2)n元素与f元素分别是F和Br,二者的核电荷数之差是35-9=26。
(3)同周期自左向右,原子半径逐渐逐渐,同主族自上而下原子半径逐渐增大。所以原子半径最大的是K。
(4)j、d分别是硅和N,N的非金属性强于硅的。而非金属性越强,相应氢化物的稳定性越强,所以氢化物的稳定性是NH3 > SiH4。
(5)c2a4与n的单质分别是乙烯和单质溴,二者发生加成反应,方程式为CH2=CH2+Br2 →CH2BrCH2Br。
(6)c5a12是戊烷,共有3种同分异构体,分别是CH3CH2CH2CH2CH3、CH3CH2CH(CH3)2、C(CH3)4 。

(分)下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
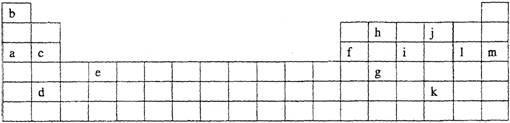
如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响:
A.原子核对核外电子的吸引力 B.形成稳定结构的倾向
下表是一些气态原子失去核外不同电子所需的能量(kJ·mol-1):
| 锂 | X | Y | |
| 失去第一个电子 | 519 | 502 | 580 |
| 失去第二个电子 | 7296 | 4570 | 1820 |
| 失去第三个电子 | 11799 | 6920 | 2750 |
| 失去第四个电子 | 9550 | 11600 |
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量。 。
②表中X可能为以上13种元素中的 (填写字母)元素。用元素符号表示X和j形成化合物的化学式 。
③Y是周期表中 族元素。
④以上13种元素中, (填写字母)元素原子失去核外第一个电子需要的能量最多。
( 13分)下表是元素周期表的一部分,请回答有关问题:(用元素符号)
| | IA | ⅡA | | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 | |
| 1 | a | | b | |||||||
| 2 | | | | | c | d | e | f | g | |
| 3 | h | | i | j | | | k | l | ||
| 4 | m | | | | | | n | | ||
(2)n元素与f元素两者核电荷数之差是_____________________;
(3)上表中,原子半径最大的是(稀有气体除外)________________;
(4)推测j、d最简单氢化物的稳定性强弱关系____________(填化学式)。
(5)c2a4与n的单质反应的化学方程式______________________________;
(6)写出c5a12的所有同分异构体的结构简式_________________________。
(共13分)下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | | | | ① | ② | ③ | | |
| 3 | ④ | | ⑤ | | | ⑥ | ⑦ | ⑧ |
| 4 | ⑨ | | | | | | | |
(2) 在最高价氧化物的水化物中,酸性最强的化合物的分子式是_______,碱性最强的化合物的电子式是:_____________。
(3) 最高价氧化物是两性氧化物的元素是_________;写出它的氧化物与氢氧化钠反应的离子方程式_____________________________________________。
(4) 用电子式表示元素④与⑥的化合物的形成过程: ,该化合物属于 (填 “共价”或“离子”)化合物。
(5)表示①与⑦的化合物的电子式 ,该化合物是由
(填“极性”“非极性”)键形成的。
(6)写出元素⑦的单质与水反应的离子方程式
(共13分)下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
|
主族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0族 |
|
2 |
|
|
|
① |
② |
③ |
|
|
|
3 |
④ |
|
⑤ |
|
|
⑥ |
⑦ |
⑧ |
|
4 |
⑨ |
|
|
|
|
|
|
|
(1) 在这些元素中,化学性质最不活泼的是: (填具体元素符号,下同)。
(2) 在最高价氧化物的水化物中,酸性最强的化合物的分子式是_______,碱性最强的化合物的电子式是:_____________。
(3) 最高价氧化物是两性氧化物的元素是_____ ____;写出它的氧化物与氢氧化钠反应的离子方程式_____ _________ _________ _________ _________ ____。
(4) 用电子式表示元素④与⑥的化合物的形成过程: ,该化合物属于 (填 “共价”或“离子”)化合物。
(5)表示①与⑦的化合物的电子式 ,该化合物是由
(填“极性”“非极性”)键形成的。
(6)写出元素⑦的单质与水反应的离子方程式