题目内容
下列电子式正确的是( )
分析:根据电子式的书写规则判断,共价化合物和非金属多原子分子的电子式书写,不仅要写共用电子对还要写各原子最外层上的孤对电子.
解答:解:A、氮气分子的电子式没写出氮原子上的孤对电子,故A错误.
B、四氯化碳中Cl原子周围有8个电子,没有标出来,故B错误.
C、氮气分子的电子式为: ,故C正确.
,故C正确.
D、二氧化碳中C与O之间各有2对电子,其电子式为: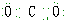 ,故D错误.
,故D错误.
故选C
B、四氯化碳中Cl原子周围有8个电子,没有标出来,故B错误.
C、氮气分子的电子式为:
 ,故C正确.
,故C正确.D、二氧化碳中C与O之间各有2对电子,其电子式为:
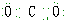 ,故D错误.
,故D错误.故选C
点评:判断型选择题的做法是:根据正确的书写方式判断选项是否正确.共价化合物和非金属多原子分子的电子式书写,不仅要写共用电子对还要写各原子最外层上的孤对电子.

练习册系列答案
相关题目
下列电子式正确的是( )
A、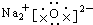 | B、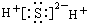 | C、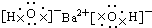 | D、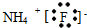 |
氰(CN)2、氧氰(OCN)2、硫氰(SCN)2、硒氰(SeCN)2的性质相似,在化学上称为拟卤素,CN-、OCN-、SCN-、SeCN一的性质与卤离子相似,已知(OCN)2的电子式为: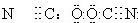 ,则下列电子式正确的是( )
,则下列电子式正确的是( )
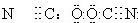 ,则下列电子式正确的是( )
,则下列电子式正确的是( )A、(CN)2  | B、OCN- 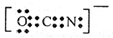 | C、SCN一 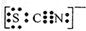 | D、SeCN-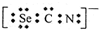 |