题目内容
【题目】分别称取2.39g(NH4)2SO4和NH4Cl固体混合物两份。
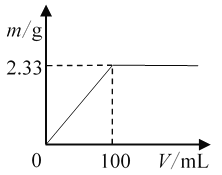
(1)将其中一份配成溶液,逐滴加入一定浓度的Ba(OH)2溶液,产生的沉淀质量与加入Ba(OH)2溶液体积的关系如图。混合物中n[(NH4)2SO4]∶n(NH4Cl)为________。
(2)另一份固体混合物中NH与Ba(OH)2溶液(浓度同上)恰好完全反应时,溶液中c(Cl-)=________(溶液体积变化忽略不计)。
【答案】1:20.100mol·Lˉ1
【解析】
(1)分别称取2.39g(NH4)2SO4和NH4Cl固体混合物两份,而第一份加100ml的氢氧化钡生成沉淀硫酸钡的质量为2.33g,其物质的量为:![]() =0.01mol,根据硫酸根离子守恒,所以第一份中硫酸铵的物质的量为0.01mol,其质量为:0.01×132=1.32g,则每份中NH4Cl的质量为:2.39-1.32=1.07g,所以氯化铵的物质的量为
=0.01mol,根据硫酸根离子守恒,所以第一份中硫酸铵的物质的量为0.01mol,其质量为:0.01×132=1.32g,则每份中NH4Cl的质量为:2.39-1.32=1.07g,所以氯化铵的物质的量为![]() =0.02mol,所以两者的物质的量之比为:0.01:0.02=1:2,故答案为:1:2;
=0.02mol,所以两者的物质的量之比为:0.01:0.02=1:2,故答案为:1:2;
(2)由(1)可知100ml氢氧化钡的物质的量为:0.01mol,所以氢氧化钡的浓度为![]() =0.1mol/L,而2.39g(NH4)2SO4和NH4Cl固体混合物中铵根离子的物质的量为:0.01×2+0.02=0.04mol,根据NH4++OH-=NH3↑+H2O可知,氢氧化钡的物质的量为:0.02mol,所以需氢氧化钡的体积为:
=0.1mol/L,而2.39g(NH4)2SO4和NH4Cl固体混合物中铵根离子的物质的量为:0.01×2+0.02=0.04mol,根据NH4++OH-=NH3↑+H2O可知,氢氧化钡的物质的量为:0.02mol,所以需氢氧化钡的体积为:![]() =0.2L,反应中氯离子的物质的量不变,2.39g(NH4)2SO4和NH4Cl固体混合物中氯化铵的物质的量为0.02mol,则c(Cl-) =
=0.2L,反应中氯离子的物质的量不变,2.39g(NH4)2SO4和NH4Cl固体混合物中氯化铵的物质的量为0.02mol,则c(Cl-) =![]() =0.1mol/L,故答案为:0.1mol/L。
=0.1mol/L,故答案为:0.1mol/L。

 名校课堂系列答案
名校课堂系列答案【题目】如图W、X、Y、Z为四种物质,若箭头表示能一步转化的常见反应,其中常温下能实现图示转化关系的是
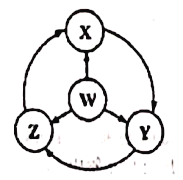
选项 | W | X | Y | Z |
A | Fe | Fe(OH)2 | FeCl3 | FeCl2 |
B | Na | Na202 | NaOH | NaCl |
C | S | SO2 | SO3 | H2SO4 |
D | A1 | AlCl3 | NaAlO2 | Al2(SO4)3 |
A. A B. B C. C D. D