题目内容
下列有关离子反应或离子方程式的叙述中,正确的是( )
| A.能使pH试纸显深红色的溶液中,Fe3+、Cl-、Ba2+、Br-能大量共存 |
B.惰性电极电解氯化铝溶液:2Cl-+2H2O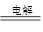 Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
| C.镁与极稀硝酸反应生成硝酸铵的离子方程式为4Mg+6H++NO3—=4Mg2++NH4++3H2O |
| D.将10 mL 0.1 mol·L-1 KAl(SO4)2溶液和10 mL 0.2 mol·L-1Ba(OH)2溶液混合,得到的沉淀中Al(OH)3和BaSO4的物质的量之比为1∶2 |
A
解析

练习册系列答案
相关题目
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.c(H+)=1.0×10-12mol·L-1的溶液:K+、Mg2+、CH3COO一、Br— |
| B.甲基橙呈红色的溶液:NH4+、Ba2+、NO3一、Cl一 |
| C.与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- |
| D.含1.0 mol·L-1 KNO3的溶液:Cl-、SO42-、H+、Fe2+ |
下列各表述与示意图一致的是( )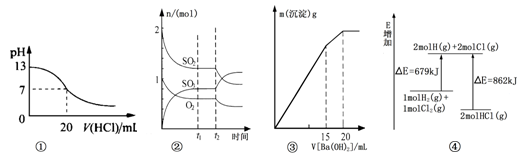
| A.图①表示25℃时,用0.1 mol/L盐酸滴定20 mL 0.1 mol/L NaOH溶液,溶液的pH随加入酸体积的变化得到的滴定曲线 |
B.图②表示一定条件下进行的反应2SO2(g) + O2(g) 2SO3(g) ΔH < 0各成分的物质的量变化,t2时刻改变的条件可能是降低温度或缩小容器体积 2SO3(g) ΔH < 0各成分的物质的量变化,t2时刻改变的条件可能是降低温度或缩小容器体积 |
| C.图③表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20 mL Ba(OH)2溶液时铝离子恰好沉淀完全 |
| D.图④表示化学反应H2(g)+C12(g)==2HCl(g)的能量变化,则该反应的反应热△H=﹢183 kJ/mol |
下列有关化学用语的表示正确的是
A.中子数为20的氯原子符号为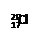 |
| B.乙烯的结构简式为CH2CH2 |
| C.C60和石墨互为同位素 |
| D.NaHCO3的电离方程式为NaHCO3=Na++ HCO3- |
能正确表示下列反应的离子方程式是( )
| A.浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑ |
| B.钠与CuSO4溶液反应:2Na+Cu2+=Cu↓+2Na+ |
| C.NaHCO3溶液与稀H2SO4反应:CO32-+2H+=H2O+CO2↑ |
| D.向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ |
下列表示对应化学反应的离子方程式正确的是( )
A.MnO2与浓盐酸反应制Cl2:MnO2+4HCl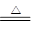 Mn2++2Cl-+Cl2↑+2H2O Mn2++2Cl-+Cl2↑+2H2O |
| B.明矾溶于水产生Al(OH)3胶体:Al3++3H2O=Al(OH)3↓+3H+ |
| C.Na2O2溶于水产生O2:Na2O2+H2O=2Na++2OH-+O2↑ |
| D.Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3—+Ca2++OH-=CaCO3↓+H2O |
下列离子方程式书写正确的是( )
A.铜溶于浓硝酸:Cu+4HNO3(浓) Cu2++2NO2↑+2H2O Cu2++2NO2↑+2H2O |
B.硫酸铁溶液与氢氧化钡溶液混合:Fe3++S +Ba2++3OH- +Ba2++3OH- Fe(OH)3↓+BaSO4↓ Fe(OH)3↓+BaSO4↓ |
C.次氯酸钙溶液中通入过量的CO2:ClO-+H2O+CO2 HC HC +HClO +HClO |
D.碳酸氢镁与足量的石灰水反应:Mg2++2HC +2OH-+Ca2+ +2OH-+Ca2+ CaCO3↓+MgCO3↓+2H2O CaCO3↓+MgCO3↓+2H2O |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A.0.1 mol·L-1的NaI溶液:K+、H+、SO42—、NO3— |
| B.0.1 mol·L-1的NaHCO3溶液:K+、Na+、NO3—、Cl- |
| C.0.1 mol·L-1 FeCl3溶液:K+、Na+、ClO-、Cl- |
| D.0.1 mol·L-1的氨水:Cu2+、Na+、SO42—、NO3— |
甲、乙、丙、丁四种易溶于水的物质,分别由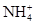 、Ba2+、Mg2+、H+、OH-、Cl-、
、Ba2+、Mg2+、H+、OH-、Cl-、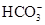 、
、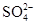 中的不同阳离子和阴离子各一种组成,已知:
中的不同阳离子和阴离子各一种组成,已知:
①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;②0.1 mol/L乙溶液中c(H+)>0.1 mol/L;③向丙容器中滴入AgNO3溶液有不溶于稀硝酸的白色沉淀生成,下列结论不正确的是( )
| A.甲溶液含有Ba2+ | B.乙溶液含有SO42+ |
| C.丙溶液含有Cl- | D.丁溶液含有Mg2+ |