题目内容
【题目】四种短周期元素X、Y、Z和W在周期表中的位置如图所示,原子序数之和为48。下列说法不正确的是
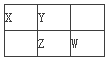
A. 原子半径(r)大小比较r(X)>r(Y)
B. X和W可形成化合物XW3
C. W的非金属性比Z的强,所以W氢化物的沸点比Z的高
D. Z的最低价单核阴离子的失电子能力比Y的强
【答案】C
【解析】
X、Y、Z、W四种短周期元素,由位置可知,X、Y在第二周期,Z、W在第三周期,设Y的原子序数为y,则X的原子序数为y-1,Z的原子序数为y+8,W的原子序数为y+9,X、Y、Z和W的原子序数之和为48,则y-1+y+y+8+y+9=48,解得y=8,所以Y为O,Z为S,W为Cl,X为N,则
A、在同一周期内,自左向右原子半径逐渐减小,原子半径(r)大小比较r(X)>r(Y),故A正确;
B、X为N元素,W为Cl元素,可以形成共价化合物NCl3,故B正确;
C、熔沸点为物质的物理性质,氢化物的沸点与分子间作用力有关,与非金属性无关,故C错误;
D、非金属性Z<Y,故Z的最低价单核阴离子的失电子能力强于Y,故D正确。
综上所述,答案选C。

练习册系列答案
相关题目
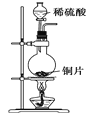
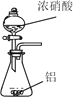
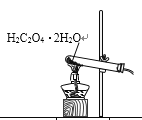
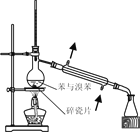
【题目】已知草酸晶体(H2C2O4·2H2O)的熔点为101℃,170℃分解。下列选用的装置和药品能达到实验目的的是
A | B | C | D |
|
|
|
|
制取SO2 | 制取NO2 | H2C2O4·2H2O分解 | 分离苯与溴苯 |
A. A B. B C. C D. D