题目内容
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.澄清透明溶液中:Cl-、NO3-、Cu2+、NH4+ |
| B.水电离产生的c(OH-)=1×10-11mol/L的溶液:Cu 2+、SO42-、NO3-、Cl- |
| C.中性溶液中:Fe3+、Al3+、NO3-、SO42- |
| D.能使苯酚变紫色的溶液:K+、Mg2+、S2-、SO42- |
A
解析试题分析:B、由题目条件可得水的电离被抑制,溶液可能为酸溶液,也可能为碱溶液,当为碱溶液时,铜离子和氢阳根离子反应,故在溶液中不能大量共存,B错误;C、在中性溶液中,铁离子早已水解完全,故铁离子不存在,C错误;D、能使苯酚变紫色的溶液中含铁离子,铁离子和硫离子因发生氧化还原反应而不能在溶液中大量共存,故错误;故选A。
考点:离子共存

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
某无色透明的酸性溶液中能大量共存的一组离子是( )
| A.Mg2+、Na+、SO42-、NO 3- | B.Na+、HCO3-、K+、SO42- |
| C.MnO4-、K+、SO42-、Na+ | D.NH4+、CO32-、Al3+、Cl- |
下列化学反应的离子方程式正确的是
| A.FeCl3与氨水反应:Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+ |
B.铜与稀硝酸反应:Cu+8H++2NO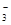 =Cu2++2NO↑+4H2O =Cu2++2NO↑+4H2O |
| C.NO2与水反应:3NO2+H2O=NO3-+NO+2H+ |
| D.醋酸与CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
下列离子方程式正确的是
| A.硫酸铜溶液与足量氢氧化钡溶液混合:Ba2++SO42-=BaSO4↓ |
| B.AgCl悬浊液中加入硫化钠饱和溶液:2AgCl + S2-=Ag2S +2Cl- |
C.硫化钠的水解反应:S2-+H3O+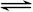 HS-+H2O HS-+H2O |
| D.用K37ClO3与浓盐酸制氯气:37ClO3-+6H++6Cl-=37Cl-+3Cl2↑+3H2O |
下列离子方程式与所述事实相符且正确的是( )
| A.漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO3- |
| B.向Na2SO3溶液中通入足量氯气:SO32-+Cl2+H2O=SO42-+2Cl-+2H+ |
| C.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-=Mn2++Cl2↑+2H2O |
| D.钠与CuSO4溶液反应:2Na+Cu2+===Cu+2Na+ |
能正确表示下列反应的离子方程式的是
| A.NaOH溶液中加入铝片:Al+2OH-=AlO2-+H2↑ |
B.NaHCO3溶液水解:HCO3-+H2O H3O+ +CO32- H3O+ +CO32- |
| C.NH4HCO3溶液与足量烧碱溶液混合:HCO3-+OH-=CO32-+H2O |
| D.硫酸溶液与氢氧化钡溶液混合:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
下列各组离子中,在强碱性溶液中能大量共存是
| A.Na+、HCO3-、CO32-、K+ | B.K+、Ba2+、Cl-、NO3- |
| C.Na+、NO3-、K+、S2- | D.K+、NH4+、SO42-、Cl- |
水溶液中能大量共存的一组离子是
| A.Na+、Ca2+、Cl-、SO42- |
| B.Fe2+、H+ 、SO32-、ClO- |
| C.Mg2+、NH4+、Cl-、SO42- |
| D.K+、Fe3+、NO3-、SCN- |