题目内容
在宇宙飞船中,为了使宇航员得到良好的生存环境,一般在飞船机内安装了盛有Na2O2颗粒的装置,它的用途是再生O2,如果用KO2代替Na2O2也能达到同样的目的,反应产物也很相似.
(1)写出KO2与CO2反应的化学方程式
(2)计算用Na2O2和KO2分别与CO2反应,产生等量的氧气,所需Na2O2和KO2的质量比为
(1)写出KO2与CO2反应的化学方程式
4KO2+2CO2=2K2CO3+3O2
4KO2+2CO2=2K2CO3+3O2
;(2)计算用Na2O2和KO2分别与CO2反应,产生等量的氧气,所需Na2O2和KO2的质量比为
1.6
1.6
.(精确到小数点后的一位小数).分析:(1)根据题意可知,KO2与CO2反应生成碳酸钾和氧气,以此书写反应的化学方程式;
(2)根据反应的化学方程式计算;
(2)根据反应的化学方程式计算;
解答:解:(1)根据题意可知,“用KO2代替Na2O2也能达到同样的目的,反应产物也很相似”,
则KO2与CO2反应生成碳酸钾和氧气,反应的方程式为4KO2+2CO2=2K2CO3+3O2,
故答案为:4KO2+2CO2=2K2CO3+3O2;
(2)设生成3mol氧气,则
4KO2+2CO2=2K2CO3+3O2
4mol 3mol
n(KO2)=4mol
m(KO2)=4mol×71g/mol=284g,
2Na2O2+=2Na2CO3+O2
2 1
6mol 3mol
n(Na2O2)=6mol
m(Na2O2)=6mol×78g/mol=468g,
所以产生等量的氧气,所需Na2O2和KO2的质量比为:
=1.6,
故答案为:1.6.
则KO2与CO2反应生成碳酸钾和氧气,反应的方程式为4KO2+2CO2=2K2CO3+3O2,
故答案为:4KO2+2CO2=2K2CO3+3O2;
(2)设生成3mol氧气,则
4KO2+2CO2=2K2CO3+3O2
4mol 3mol
n(KO2)=4mol
m(KO2)=4mol×71g/mol=284g,
2Na2O2+=2Na2CO3+O2
2 1
6mol 3mol
n(Na2O2)=6mol
m(Na2O2)=6mol×78g/mol=468g,
所以产生等量的氧气,所需Na2O2和KO2的质量比为:
| 468 |
| 284 |
故答案为:1.6.
点评:本题考查碱金属的重要化合物,题目难度不大,注意把握题目信息,具有一定的知识迁移能力,把握有关反应的方程式的书写.

练习册系列答案
相关题目
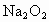 颗粒的装置,它的用途是再生
颗粒的装置,它的用途是再生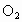 ,如果用
,如果用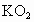 代替
代替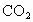 反应的化学方程式__________________________.
反应的化学方程式__________________________.