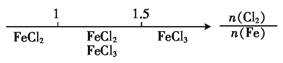
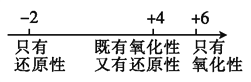
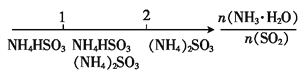题目内容
【题目】下列说法正确的是
A. 某物质的溶解性为难溶,则该物质不溶于水
B. H2S为二元弱酸,其电离方程式为:H2S![]() 2H++S2-
2H++S2-
C. 已知:常温下,AgCl的Ksp=1.8×10-10。向99mL 0.01 mol/L KCl溶液中,加入lmL 0.01mol/LAgNO3溶液(忽略混合时溶液体积的变化),立即产生白色沉淀
D. NaHCO3溶于水会水解,该水解反应可表示为:HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
【答案】C
【解析】A.室温(即20℃)时的溶解度小于0.01g的,叫难溶(或不溶)物质,绝对不溶的物质是没有的,故A错误;B.H2S为二元弱酸,其电离分步进行,故B错误;C.Qc=c(Cl-)×c(Ag+)=0.01mol/L×0.01mol/L=1×10-4>Ksp,则立即产生白色沉淀,故C正确;D.NaHCO3溶于水会水解,该水解反应可表示为:HCO3-+H2O![]() OH-+H2CO3,故D错误;答案为C。
OH-+H2CO3,故D错误;答案为C。

练习册系列答案
相关题目