题目内容
甲、乙、丙三种物质之间有如下转化关系:
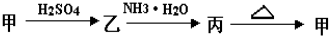
(1)若甲是不溶于水的白色固体物质,既能溶于盐酸又能溶于氢氧化钠溶液,则甲是______ 写出乙丙转化的化学方程式:______.
(2)若乙溶液中加入KSCN溶液,有血红色出现,则甲物质是______.写出 甲乙转化的离子方程式______.
解:(1)通过题意知,甲是两性物质,我们学过的既能溶于酸又能溶于碱的物质有铝、氧化铝、氢氧化铝.通过转化方式得,甲、乙、丙有相同的元素.无论是哪种物质由甲生成乙,乙都是硫酸铝,硫酸铝和氨水反应生成氢氧化铝,氢氧化铝加热分解的氧化铝,所以甲是Al2O3,乙丙转化属于复分解反应,盐和碱反应生成另外的盐和碱,所以方程式为:
Al2(SO4)3+6NH3?H2O=2Al(OH)3+3(NH4)2SO4,故答案为:Al2O3;Al2(SO4)3+6NH3?H2O=2Al(OH)3+3(NH4)2SO4;
(2)通过转化方式得,甲、乙、丙有相同的元素,甲与硫酸反应生成乙,乙是硫酸盐,硫酸盐与氨水反应生成丙,丙是不溶性的碱,碱加热分解的氧化物,所以甲是氧化物.若乙溶液中加入KSCN溶液,有血红色出现,有血红色出现是Fe3+的特征反应所以甲是Fe2O3,氧化物和酸反应生成盐和水,所以其离子方程式为:Fe2O3+6H+=2Fe3++3H2O,
故答案为:Fe2O3;Fe2O3+6H+=2Fe3++3H2O.
分析:(1)通过题意知,甲是两性物质,我们学过的既能溶于酸又能溶于碱的物质有铝、氧化铝、氢氧化铝.通过转化方式得,甲、乙、丙有相同的元素.无论是哪种物质由甲生成乙,乙都是硫酸铝,硫酸铝和氨水反应生成氢氧化铝,氢氧化铝加热分解的氧化铝,所以甲是Al2O3;
(2)通过转化方式得,甲、乙、丙有相同的元素,加入KSCN溶液,有血红色出现是Fe3+的特征反应,所以甲是Fe2O3.
点评:本题考查的是金属及其化合物的性质,解答时根据物质的特殊性质进行推断、分析,然后再根据推断进行验证是否符合题意.一些物质的特征现象:Fe2+在溶液中呈绿色、Fe3+在溶液中呈黄色、Cu2+在溶液中呈蓝色;一些特征反应:醛的检验、二氧化硫的漂白性、铵根离子的检验、乙醇的检验等.
Al2(SO4)3+6NH3?H2O=2Al(OH)3+3(NH4)2SO4,故答案为:Al2O3;Al2(SO4)3+6NH3?H2O=2Al(OH)3+3(NH4)2SO4;
(2)通过转化方式得,甲、乙、丙有相同的元素,甲与硫酸反应生成乙,乙是硫酸盐,硫酸盐与氨水反应生成丙,丙是不溶性的碱,碱加热分解的氧化物,所以甲是氧化物.若乙溶液中加入KSCN溶液,有血红色出现,有血红色出现是Fe3+的特征反应所以甲是Fe2O3,氧化物和酸反应生成盐和水,所以其离子方程式为:Fe2O3+6H+=2Fe3++3H2O,
故答案为:Fe2O3;Fe2O3+6H+=2Fe3++3H2O.
分析:(1)通过题意知,甲是两性物质,我们学过的既能溶于酸又能溶于碱的物质有铝、氧化铝、氢氧化铝.通过转化方式得,甲、乙、丙有相同的元素.无论是哪种物质由甲生成乙,乙都是硫酸铝,硫酸铝和氨水反应生成氢氧化铝,氢氧化铝加热分解的氧化铝,所以甲是Al2O3;
(2)通过转化方式得,甲、乙、丙有相同的元素,加入KSCN溶液,有血红色出现是Fe3+的特征反应,所以甲是Fe2O3.
点评:本题考查的是金属及其化合物的性质,解答时根据物质的特殊性质进行推断、分析,然后再根据推断进行验证是否符合题意.一些物质的特征现象:Fe2+在溶液中呈绿色、Fe3+在溶液中呈黄色、Cu2+在溶液中呈蓝色;一些特征反应:醛的检验、二氧化硫的漂白性、铵根离子的检验、乙醇的检验等.

练习册系列答案
相关题目




 、
、 、
、



