题目内容
(2013?安徽模拟)实验室可以用MgCl2?6H20为原料制备碳酸镁晶须,主要流程如下:
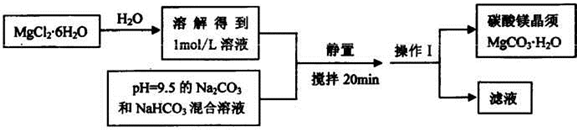
试回答:
(1)操作1的名称是
(2)上述反应过程要控制好温度,因为MgCO3置于水中长时间加热煮沸可完全生成 Mg(OH)2.其原因是
(3)另査阅文献,在加热煮沸时也可能生成碱式碳酸镁Mg(OH)2(CO3)4?4H2O,写出该反应的化学方程式
(4)某课题组为了确定MgCO3在水中长时间加热煮沸后所得的固体成分,进行如下 研究.(注:Mg(OH)2,Mg5(OH)2(CO3)4.4H2O在煮沸时均不会分解)
①定性研究:请你完成下表中内容.
②另取一定质量的固体,灼烧至恒重,能否通过固体质惫的减少量来确定固体的成分?

试回答:
(1)操作1的名称是
过滤
过滤
.(2)上述反应过程要控制好温度,因为MgCO3置于水中长时间加热煮沸可完全生成 Mg(OH)2.其原因是
MgCO3在加热煮沸过程中能发生水解反应.由于水解生成的Mg(OH)2溶解度更小,且又有CO2气体生成,使水解趋于完全,MgCO3转化为Mg(OH)2
MgCO3在加热煮沸过程中能发生水解反应.由于水解生成的Mg(OH)2溶解度更小,且又有CO2气体生成,使水解趋于完全,MgCO3转化为Mg(OH)2
.(3)另査阅文献,在加热煮沸时也可能生成碱式碳酸镁Mg(OH)2(CO3)4?4H2O,写出该反应的化学方程式
5 MgCO3+5H2O
Mg5(OH)2(CO3)4?4H2O+CO2↑
| ||
5 MgCO3+5H2O
Mg5(OH)2(CO3)4?4H2O+CO2↑
.
| ||
(4)某课题组为了确定MgCO3在水中长时间加热煮沸后所得的固体成分,进行如下 研究.(注:Mg(OH)2,Mg5(OH)2(CO3)4.4H2O在煮沸时均不会分解)
①定性研究:请你完成下表中内容.
| 实验步骤 | 预期的实验现象和结论 |
| 取一定质量的固体样品 置于试管中,滴加足量的稀盐酸 (或置于试管中充分加热,将产生的气体通入到盛有足量澄清石灰水的烧杯) 置于试管中,滴加足量的稀盐酸 (或置于试管中充分加热,将产生的气体通入到盛有足量澄清石灰水的烧杯) |
若 无气泡生成 (或澄清石灰水不变浑浊 ) 无气泡生成 ,则固体产物为Mg(OH)2(或澄清石灰水不变浑浊 ) |
能
能
(填“能”或“否”),理由是等质量的氢氧化镁或碱式碳酸镁灼烧至恒重时,固体质量的减少量是确定的,且不相同
等质量的氢氧化镁或碱式碳酸镁灼烧至恒重时,固体质量的减少量是确定的,且不相同
.分析:(1)从溶液中分离出固体,应用过滤的方法;
(2)Mg(OH)2溶解度比小MgCO3,且MgCO3水解;
(3)根据反应物和生成物结合质量守恒定律书写方程式;
(4)确定MgCO3在水中长时间加热煮沸后所得的固体成分,可加入盐酸,如生成气泡,说明含有碳酸镁或碱式碳酸镁,否则为Mg(OH)2,可根据物质灼烧前后质量的变化确定物质的组成.
(2)Mg(OH)2溶解度比小MgCO3,且MgCO3水解;
(3)根据反应物和生成物结合质量守恒定律书写方程式;
(4)确定MgCO3在水中长时间加热煮沸后所得的固体成分,可加入盐酸,如生成气泡,说明含有碳酸镁或碱式碳酸镁,否则为Mg(OH)2,可根据物质灼烧前后质量的变化确定物质的组成.
解答:解:(1)从溶液中分离出固体,应用过滤的方法,故答案为:过滤;
(2)MgCO3在加热煮沸过程中能发生水解反应,发生MaCO3+H2O
Mg(OH)2↓+CO2↑,水解生成的Mg(OH)2溶解度更小,加热促进水解,MgCO3转化为Mg(OH)2,
故答案为:MgCO3在加热煮沸过程中能发生水解反应.由于水解生成的Mg(OH)2溶解度更小,且又有CO2气体生成,使水解趋于完全,MgCO3转化为Mg(OH)2;
(3)MgCO3在加热煮沸过程中能生成Mg(OH)2(CO3)4?4H2O,反应的方程式为5 MgCO3+5H2O
Mg5(OH)2(CO3)4?4H2O+CO2↑,
故答案为:5 MgCO3+5H2O
Mg5(OH)2(CO3)4?4H2O+CO2↑;
(4)①确定MgCO3在水中长时间加热煮沸后所得的固体成分,可加入盐酸,如生成气泡,说明含有碳酸镁或碱式碳酸镁,否则为Mg(OH)2,可取一定质量的固体样品置于试管中,滴加足量的稀盐酸(或置于试管中充分加热,将产生的气体通入到盛有足量澄清石灰水的烧杯),如无气泡生成(或澄清石灰水不变浑浊),可证明固体产物为
Mg(OH)2,
故答案为:
;
②等质量的氢氧化镁或碱式碳酸镁灼烧至恒重时,固体质量的减少量是确定的,且不相同,可通过固体灼烧至恒重,根据质量差值可确定固体的成分,
故答案为:能;等质量的氢氧化镁或碱式碳酸镁灼烧至恒重时,固体质量的减少量是确定的,且不相同.
(2)MgCO3在加热煮沸过程中能发生水解反应,发生MaCO3+H2O
| ||
故答案为:MgCO3在加热煮沸过程中能发生水解反应.由于水解生成的Mg(OH)2溶解度更小,且又有CO2气体生成,使水解趋于完全,MgCO3转化为Mg(OH)2;
(3)MgCO3在加热煮沸过程中能生成Mg(OH)2(CO3)4?4H2O,反应的方程式为5 MgCO3+5H2O
| ||
故答案为:5 MgCO3+5H2O
| ||
(4)①确定MgCO3在水中长时间加热煮沸后所得的固体成分,可加入盐酸,如生成气泡,说明含有碳酸镁或碱式碳酸镁,否则为Mg(OH)2,可取一定质量的固体样品置于试管中,滴加足量的稀盐酸(或置于试管中充分加热,将产生的气体通入到盛有足量澄清石灰水的烧杯),如无气泡生成(或澄清石灰水不变浑浊),可证明固体产物为
Mg(OH)2,
故答案为:
| 实验步骤 | 预期的实验现象和结论 |
| 置于试管中,滴加足量的稀盐酸 (或置于试管中充分加热,将产生的气体通入到盛有足量澄清石灰水的烧杯) |
无气泡生成 (或澄清石灰水不变浑浊 ) |
②等质量的氢氧化镁或碱式碳酸镁灼烧至恒重时,固体质量的减少量是确定的,且不相同,可通过固体灼烧至恒重,根据质量差值可确定固体的成分,
故答案为:能;等质量的氢氧化镁或碱式碳酸镁灼烧至恒重时,固体质量的减少量是确定的,且不相同.
点评:本题考查制备实验方案的设计,侧重于盐类水解的应用的考查,注意把握实验的原理和操作方法,为高考常见题型,易错点为(4),注意根据物质的性质设计实验方案.

练习册系列答案
相关题目
 (2013?安徽模拟)由碳原子构成的纳米碳管可以作为储存氢气的优良容器,其单层部分结构示意图如图,下列说法正确的是( )
(2013?安徽模拟)由碳原子构成的纳米碳管可以作为储存氢气的优良容器,其单层部分结构示意图如图,下列说法正确的是( )