题目内容
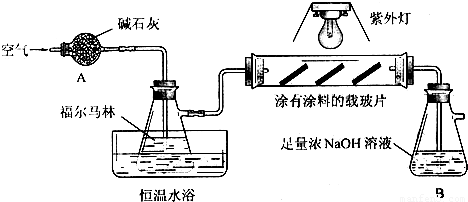
室内甲醛污染已被列入对公众健康影响最大的环境因素之一,市面上有一种光催化涂料,能够起到降低室内甲醛含量的作用.某化学兴趣小组想要通过此涂料来进行甲醛的光催化氧化反应,并测定被氧化的甲醛的量.设计实验装置如下:
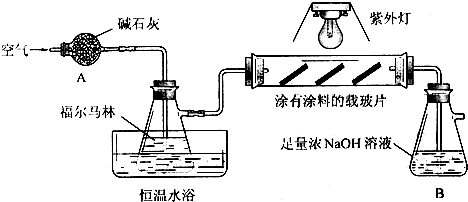
实验时先开启紫外灯,缓缓鼓入空气;一段时间后停止反应,关闭紫外灯,再继续通入一会儿空气,向B中加入足量BaCl2溶液,得到白色沉淀5.91g.
(1)福尔马林是催化氧化甲醇制得的含甲醛37%的水溶液,因此含有二种有机杂质,它们是______,______,福尔马林的一个用途是______.
(2)上图装置A中,碱石灰的作用是______,恒温水浴的目的是______.
(3)硬质玻璃管中,甲醛在光催化氧化条件下的反应方程式:______;
(4)向B中加入足量BaCl2溶液后至得到5.91g白色沉淀的一系列操作依次是:过滤、______、干燥、______;过滤时需用的玻璃仪器除烧杯、玻璃棒外还有______.
(5)计算被氧化的甲醛的物质的量为______mol
(6)反应结束后,继续遭入一会儿空气的目的是______.
(7)甲同学认为,反应过程中部分甲醛可能被氧化为甲酸.为验证其存在,甲同学取B中溶液,分别选用下表试剂进行检验.但乙同学认为试剂选择均不合理,他的理由是:

实验时先开启紫外灯,缓缓鼓入空气;一段时间后停止反应,关闭紫外灯,再继续通入一会儿空气,向B中加入足量BaCl2溶液,得到白色沉淀5.91g.
(1)福尔马林是催化氧化甲醇制得的含甲醛37%的水溶液,因此含有二种有机杂质,它们是______,______,福尔马林的一个用途是______.
(2)上图装置A中,碱石灰的作用是______,恒温水浴的目的是______.
(3)硬质玻璃管中,甲醛在光催化氧化条件下的反应方程式:______;
(4)向B中加入足量BaCl2溶液后至得到5.91g白色沉淀的一系列操作依次是:过滤、______、干燥、______;过滤时需用的玻璃仪器除烧杯、玻璃棒外还有______.
(5)计算被氧化的甲醛的物质的量为______mol
(6)反应结束后,继续遭入一会儿空气的目的是______.
(7)甲同学认为,反应过程中部分甲醛可能被氧化为甲酸.为验证其存在,甲同学取B中溶液,分别选用下表试剂进行检验.但乙同学认为试剂选择均不合理,他的理由是:
| 甲同学选择的试剂 | 乙同学认为不合理的理由 |
| 紫色石蕊试液 | ______ |
| 新制氢氧化铜 | ______ |
(1)甲醇催化氧化得到甲酸,福尔马林中含有甲醛、甲醇、甲酸,可用于浸制生物标本,故答案为:甲醇;甲酸;浸制生物标本(杀菌剂等,合理即可);
(2)碱石灰可吸收空气中的二氧化碳;恒温水浴可使甲醛挥发,故答案为:吸收空气中的CO2(防止对产物检验测定造成干扰);使混合气中甲醛含量稳定(写使甲醛挥发亦可);
(3)甲醛在光催化氧化条件下反应生成二氧化碳和水,反应方程式HCHO+O2
CO2+H2O,故答案为:HCHO+O2
CO2+H2O;
(4)沉淀需要过滤、洗涤、干燥、称量;过滤时需用的玻璃仪器有烧杯、玻璃棒、和普通漏斗,故答案为:洗涤;称量;普通漏斗;
(5)白色沉淀为碳酸钡,物质的量为
=0.03mol,根据碳元素守恒,可知被氧化的甲醛的物质的量为0.03mol,故答案为:0.03;
(6)通入一会儿空气的目的排出装置中的二氧化碳,减小误差,故答案为:将残留在装置中的CO2排出,被NaOH吸收,减小误差;
(7)紫色石蕊试液B中溶液呈碱性(NaOH足量),无法证明是甲酸;B中可能溶有过量的甲醛,故答案为:紫色石蕊试液B中溶液呈碱性(NaOH足量),无法证明是甲酸(酸性);B中可能溶有过量的甲醛,无法证明是甲酸中醛基.
(2)碱石灰可吸收空气中的二氧化碳;恒温水浴可使甲醛挥发,故答案为:吸收空气中的CO2(防止对产物检验测定造成干扰);使混合气中甲醛含量稳定(写使甲醛挥发亦可);
(3)甲醛在光催化氧化条件下反应生成二氧化碳和水,反应方程式HCHO+O2
| 催化剂 |
| 紫外光 |
| 催化剂 |
| 紫外光 |
(4)沉淀需要过滤、洗涤、干燥、称量;过滤时需用的玻璃仪器有烧杯、玻璃棒、和普通漏斗,故答案为:洗涤;称量;普通漏斗;
(5)白色沉淀为碳酸钡,物质的量为
| 5.91g |
| 197g/mol |
(6)通入一会儿空气的目的排出装置中的二氧化碳,减小误差,故答案为:将残留在装置中的CO2排出,被NaOH吸收,减小误差;
(7)紫色石蕊试液B中溶液呈碱性(NaOH足量),无法证明是甲酸;B中可能溶有过量的甲醛,故答案为:紫色石蕊试液B中溶液呈碱性(NaOH足量),无法证明是甲酸(酸性);B中可能溶有过量的甲醛,无法证明是甲酸中醛基.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目