题目内容
用1.0 mol·L-1 NaOH溶液中和某浓度硫酸溶液时,其pH和所加NaOH溶液的体积关系如图10-9所示。原硫酸溶液的物质的量浓度和反应后溶液的总体积是( )?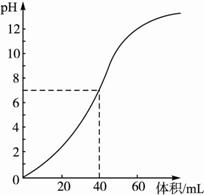
图10-9
A.1 mol·L-1,60 mL?
B.0.5 mol·L-1,80 mL?
C.0.5 mol·L-1,40 mL?
D.1 mol·L-1,80 mL
B?
解析:据图观察,开始时pH等于0,可知c(H+)=1 mol·L-1,c(H2SO4)=0.5 mol·L-1,当恰好反应时,消耗NaOH溶液体积为40 mL,根据c(H+)V(酸)=c(OH-)V(碱),已知c(NaOH)=1.0 mol·L-1,c(H+)=1.0 mol·L-1,可知:V(酸)=V(碱)=40mL,则总体积为80 mL。

练习册系列答案
相关题目