题目内容
(每空2分,共12分)仔细阅读下列三段文字
①由稀有气体元素Xe(氙)与氧元素形成的一种共价化合物XeO3极不稳定,易转化为单质而呈强氧化性。将适量的XeO3投入含Mn2+的水溶液中,溶液逐渐变为紫红色且pH不断减小。
② 将0.08mol KMnO4固体(质量为12.64g)加热一段时间后,收集到a molO2;
向反应后残留的固体中加入足量的浓盐酸,又收集到b molCl2,此时Mn元素全部以Mn2+的形式存在于溶液中。
③氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式: Cl2+2e- =2Cl-
回答问题:
(1)试写出①有关的离子方程式:_________ _______。
(2)请配平②的化学方程式:
KMnO4+ HCl - KCl+ MnCl2+ Cl2↑+ H2O
通过对第②段文字中提供的数据进行推导和计算可得出:
a +b的最大值为 ,a +b最小值为 。
(3)下列四种物质中能使③中的还原过程发生的物质是 。
A. Na2CO3 B. KMnO4 C. XeO3 D. Na2SO3
将该反应的氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并用单线桥表示电子转移的方向和数目:

(每空2分,共12分)(1)5XeO3+6Mn2++9H2O====5Xe+6MnO4-+18H+。
(2)配平 2 、 16 = 2 、 2 、 5 、 8 , 0.2 , 0.16 。
(3) D 。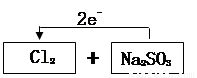
【解析】(1)溶液逐渐变为紫红色且pH不断减小,所以反应中有MnO4-和H+生成,因此反应的方程式是5XeO3+6Mn2++9H2O====5Xe+6MnO4-+18H+。
(2)根据方程式可知,锰元素的化合价从+7价降低到+2价,得到5个电子。氯元素的化合价从-1价升高到0价,失去1个电子,所以根据电子的得失守恒和质量守恒可知,配平后的计量数分别是 2 、 16 = 2 、 2 、 5 、 8;氧气是amol,氯气是bmol,所以根据电子的得失守恒可知,4a+2b=0.08×5,即a+b=0.2-a,由于a的最大值是0.04,最小值是0,所以a+b的最大值是0.2mol,最小值是0.16mol。
(3)碳酸钠没有还原性,现象B和C都具有强氧化性,能氧化氯离子,亚硫酸钠具有还原性,所以答案选D。

 如下的问题,探究。请你协助该小组的同学完成下列研究。
如下的问题,探究。请你协助该小组的同学完成下列研究。
 能被NH3还原吗?
能被NH3还原吗? 红色物质是Cu,也有同学认为NH3与CuO反应生成的红色物质
红色物质是Cu,也有同学认为NH3与CuO反应生成的红色物质 是Cu和A的混合物。请你设计一个简单的实验检验NH3与CuO反应中生成的红色物质中是否含有A______________________________________________________。
是Cu和A的混合物。请你设计一个简单的实验检验NH3与CuO反应中生成的红色物质中是否含有A______________________________________________________。