题目内容
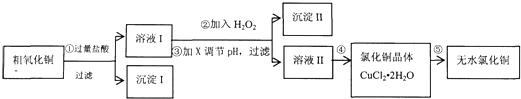
(16分)某同学拟用粗氧化铜(含少量氧化亚铁及不溶于酸的杂质)制取无水氯化铜,流程如图所示:

(1)步骤①中涉及的离子方程式有: 。
(2)步骤②中加入H2O2的目的是: 反应的离子方程式为 。
(3)已知:
|
|
氢氧化物开始沉淀时的pH |
氢氧化物沉淀完全时的pH |
|
Fe3+ |
1.9 |
3.2 |
|
Cu2+ |
4.7 |
6.7 |
|
Fe2+ |
7 |
9 |
步骤③中调节pH的最佳范围为 ,
步骤③中可以用于调节溶液pH的试剂X是 :
a.Cu2(OH)2CO3 b.CuO c. Cu(OH)2 d.NH3•H2O
(4)步骤④进行的操作是 ,过滤、洗涤、干燥。 在步骤⑤中要得到无水CuCl2,需要在 加热CuCl2·2H2O。
(16分)(1)CuO+2H+=Cu2++H2O(2分) ,FeO+2H+=Fe2++H2O(2分);
(2)将Fe2+氧化成Fe3+(2分), 2Fe2++H2O2+2H+=2Fe3++2H2O(2分);
(3)3.2至4.7(2分) ; a b c (2分);
(4)蒸发浓缩,冷却结晶(2分)。干燥的HCl气流中(2分)
【解析】】(1)氧化铜是碱性氧化物,和盐酸反应的离子方程式为CuO+2H+=Cu2++H2O。
(2)由于溶液中含有亚铁离子,而亚铁离子的沉淀pH大于铜离子的,所以应该把亚铁离子转化为铁离子而产生氢氧化铁沉淀,从而除去杂质。
(3)要沉淀铁离子而保留铜离子,则根据pH可知,应该是3.2至4.7之间。由于调节pH是不能引入杂质的,所以答案选bc。
(4)要得到氯化铜晶体,则应该是蒸发浓缩,冷却结晶,然后过滤、洗涤干燥即可。氯化铜是强酸弱碱盐,水解生成氢氧化铜和氯化氢。所以在加热过程中,应该在氯化物的气流中进行以防止CuCl2发生水解。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案(16分)某同学拟用粗氧化铜(含少量FeO及不溶于酸的杂质)制取无水氯化铜,流程如图:
(1)步骤①中氧化铜与盐酸反应的离子万程式:___________________。
(2)步骤②中加入H2O2的目的____________________________________,
沉淀II的化学式为_______________________。
(3)已知:
| | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
| Fe2+ | 7 | 9 |
a.NaOH b.CuO c.Cu(OH)2 d.

(4)步骤④的操作是___________,过滤、洗涤、干燥。
为得到无水CuCl2,步骤⑤需在干燥的HCl气流中加热
 ,原因是__________________________________________________________。
,原因是__________________________________________________________。 (16分)某同学拟用粗氧化铜(含少量氧化亚铁及不溶于酸的杂质)制取无水氯化铜,流程如图所示:
(1)步骤①中涉及的离子方程式有: 。
(2)步骤②中加入H2O2的目的是: 反应的离子方程式为 。
(3)已知:
| | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
| Fe2+ | 7 | 9 |
步骤③中可以用于调节溶液pH的试剂X是 :
a.Cu2(OH)2CO3 b.CuO c. Cu(OH)2 d.NH3?H2O
(4)步骤④进行的操作是 ,过滤、洗涤、干燥。 在步骤⑤中要得到无水CuCl2,需要在 加热CuCl2·2H2O。
(16分)某同学拟用粗氧化铜(含少量FeO及不溶于酸的杂质)制取无水氯化铜,流程如图:

(1)步骤①中氧化铜与盐酸反应的离子万程式:___________________。
(2)步骤②中加入H2O2的目的____________________________________,
沉淀II的化学式为_______________________。
(3)已知:
|
|
氢氧化物开始沉淀时的pH |
氢氧化物沉淀完全时的pH |
|
Fe3+ |
1.9 |
3.2 |
|
Cu2+ |
4.7 |
6.7 |
|
Fe2+ |
7 |
9 |
步骤③中调节pH的最佳范围为____,调节溶液pH的试剂X可以是______________:
a.NaOH
b.CuO c.Cu(OH)2
d.
(4)步骤④的操作是___________,过滤、洗涤、干燥。
为得到无水CuCl2,步骤⑤需在干燥的HCl气流中加热 ,原因是__________________________________________________________。
,原因是__________________________________________________________。