题目内容
已知乙二酸(HOOC―COOH)俗称草酸,易溶于水,为二元弱酸,酸性强于碳酸,其盐草酸钙和草酸氢钙均为白色不溶物。无色晶体H2C2O4?2H2O称为草酸晶体,其熔点为101.5℃。草酸晶体失去结晶水得无水草酸,它在157℃升华。
根据上述信息,回答下列问题。
(1)向盛有2mL饱和NaHCO3溶液的试管里加入约2mL乙二酸浓溶液,观察到的现象是________,写出该反应的离子方程式:___________________。
(2)配平乙二酸与酸性KMnO4溶液反应的离子方程式(化学计量数填入下面相应的方框内);
_____MnO4- +_____H2C2O4 +_____H+ _____Mn2+ +_____CO2↑+_____H2O
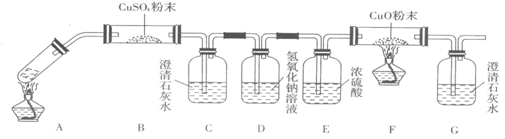
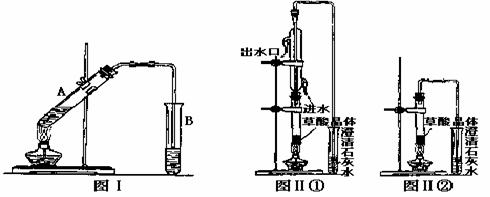
(3)向试管A中加入3mL乙醇,然后边振荡试管边加入2mL浓硫酸和2mL乙二酸溶液,按下图Ⅰ连接好装置,加热3―5min。在装有饱和Na2CO3溶液的试管B中有油状且带有香味的液体产生。B中导管口在液面上而不伸入液面下的原因是__________________。写出乙二酸与足量乙醇完全酯化的化学反应方程式__________________。

(4)已知草酸分解的化学方程式为:H2C2O4![]() H2O+CO2↑+CO↑。
H2O+CO2↑+CO↑。
利用图Ⅱ①和图Ⅱ②加热草酸晶体,以验证草酸受热是否分解。连续加热一段时间后的现象是:图Ⅱ①:试管里澄清石灰水先变浑浊,后又变澄清,其原因是___________;
图Ⅱ②:试管里澄清石灰水只变浑浊,其原因是__________;能验证草酸受热分解的装置是______(填图Ⅱ中的编号 “①”或“②”),理由是:___________(从装置的特点分析)。
(1)有无色气泡产生 ,2HCO3― + H2C2O4 = 2H2O + 2CO2↑+ C2O42―
(2) 2 5 6―2 10 8
(3)防止倒吸(或防止B中液体倒吸至A中);
![]()
(4)草酸受热分解产生CO2,CO2使澄清石灰水变浑浊,过量CO2使浑浊又变澄清; 由于大量草酸蒸气逸出,与石灰水反应生成草酸钙沉淀;①;增加了冷凝回流装置,避免草酸蒸气逸出。

 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案