题目内容
3.分离的方法:①过滤 ②蒸发 ③蒸馏 ④分液⑤萃取
请从上面选择下列各混合物的分离方法(填序号)
(1)食盐水与泥沙①
(2)海水晒盐②
(3)苯和水④
(4)蒸馏水的制取③
(5)用CCl4将碘水中的碘提取出来⑤.
分析 (1)泥沙不溶于水;
(2)海水中水的沸点较低,易挥发;
(3)苯和水分层;
(4)水的沸点低;
(5)碘不易溶于水,易溶于四氯化碳.
解答 解:(1)泥沙不溶于水,则选择过滤法分离食盐水与泥沙,故答案为:①;
(2)海水中水的沸点较低,易挥发,则选择蒸发原理进行海水晒盐,故答案为:②;
(3)苯和水分层,则选择分液法分离,故答案为:④;
(4)水的沸点低,则利用蒸馏法制备蒸馏水,故答案为:③;
(5)碘不易溶于水,易溶于四氯化碳,则利用萃取法选CCl4将碘水中的碘提取出来,故答案为:⑤.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异、混合物分离原理为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
13.下列操作中不正确的是( )
| A. | 过滤时玻璃棒与三层滤纸处接触 | |
| B. | 酒精和水的混合物可以通过蒸馏将二者分离开来 | |
| C. | 向试管中滴加液体时,胶头滴管应紧贴试管内壁 | |
| D. | KNO3中混有少量的NaCl,可通过重结晶实验将杂质出去 |
14.设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 常温下,含lmolFe的铁片与过量浓HN03反应,转移电子的数目为3NA个 | |
| B. | 电解饱和食盐水,当阴极产生2.24LH2时,转移的电子数为0.2NA | |
| C. | 标准状况下,33.6LS03含有9.03 xl023个S03分子 | |
| D. | 在46 gN02和N204的混合物气体中所含原子总数为3NA个 |
11.下列实验“操作和现象”与“结论”对应关系正确的是( )
| 操作和现象 | 结论 | |
| A | 向FeCl3和CuCl2混合溶液中加入铁粉,有红色固体析出 | 氧化性:Cu2+>Fe3+ |
| B | 用石墨作电极电解MgSO4溶液,某电极附近有白色沉淀生成 | 该电极为阳极 |
| C | 处理锅炉水垢中的CaSO4时,依次加入饱和Na2CO3溶液和盐酸,水垢溶解 | 溶度积:Ksp(CaCO3)<Ksp(CaSO4) |
| D | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有Ag+ |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
18.下列离子方程式书写正确的是( )
| A. | Na2O2投入水中:2Na2O2+2H2O=4Na++4OH-+H2↑ | |
| B. | 向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O=HClO+HSO3- | |
| C. | 钠投入CuSO4溶液中:2Na+Cu2++2H2O=2Na++Cu(OH)2↓+H2↑ | |
| D. | 铜和稀HNO3反应:3Cu+8H++2NO3-=3Cu2++2NO2↑+4H2O |
8.有一种有机化合物,其结构简式如下,下列有关它的性质叙述中,正确的是( )
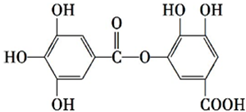

| A. | 有弱酸性,能与NaHCO3溶液反应 | |
| B. | 在一定条件下,1 mol该物质最多能与7 mol NaOH完全反应 | |
| C. | 在一定条件下,1 mol该物质可以和8 mol H2发生加成反应 | |
| D. | 能发生水解反应,水解后能生成两种物质 |
12. 金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.下列有关绿原酸的说法中不正确的是( )
金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.下列有关绿原酸的说法中不正确的是( )
 金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.下列有关绿原酸的说法中不正确的是( )
金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.下列有关绿原酸的说法中不正确的是( )| A. | 绿原酸分子中有1个手性碳原子 | |
| B. | 绿原酸分子中所有碳原子都能在同一平面上 | |
| C. | 绿原酸能发生显色反应、取代反应和加成反应 | |
| D. | 每摩尔绿原酸最多与含4molNaOH的溶液反应 |
13.下列反应中,熵变小于0的是( )
| A. | (NH4 )2CO3(s)═NH4HCO3(s)+NH3(g) | B. | 2N2O5(g)═4NO2(g)+O2(g) | ||
| C. | MgCO3(s)═MgO(s)+CO2(g) | D. | 2CO(g)═2C(s)+O2(g) |