题目内容
【题目】硒(Se),是一种非金属元素。可以用作光敏材料、电解锰行业催化剂、动物体必需的营养元素和植物有益的营养元素等。请回答下列问题:
(1) Se原子的核外电子排布式为____________。
(2) 比较As的第一电离能比Se______(填“大”或“小”)。
(3) SeO42-中Se-O的键角比SeO3的键角____(填“大”或“小”)原因是______________
(4) H2SeO4比H2SeO3水溶液的酸性___________。
(5) 硒单质是红色或灰色粉末,带灰色金属光泽的准金属,灰硒的晶体为六方晶胞结构,原子排列为无限螺旋链,分布在六方晶格上,同一条链内原子作用很强,相邻链之间原子作用较弱,其螺旋链状图、晶胞结构图和晶胞俯视图如下。
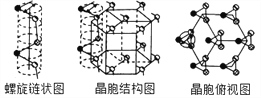
螺旋链中Se原子的杂化方式为__________。己知正六棱柱的边长为acm,高为b cm,阿伏加德罗常数为NAmol-1,则该晶胞中含有的Se原子个数为_________,该晶体的密度为___________g/cm3 (用含NA、a、b的式子表示)。
【答案】 [Ar]3d104s24p4或1s22s22p63s23p63d104s24p4 大 小 SeO42-空间构型为正四面体,键角109028,,SeO3空间构型为平面三角形,键角1200 强 SP3杂化 9 ![]()
【解析】 (1)34号元素 Se原子的核外电子排布式为 [Ar]3d104s24p4或1s22s22p63s23p63d104s24p4 ; (2)As是N族元素,p轨道是半满,是比较稳定的, 所以As的第一电离能比Se大;(3)SeO42-空间构型为正四面体,键角109028,,SeO3空间构型为平面三角形,键角1200 ,SeO42―的键角小。(4) H2SeO4含有2个非羟基氧,H2SeO3只含有1个非羟基氧,分子中非羟基氧数目越多,其水溶液的酸性越强,故H2SeO4比H2SeO3水溶液的酸性强;(5) 每个硒原子最外层6个电子,形成2个σ键,2个孤电子对,所以是SP3杂化 ;该晶胞中含有的Se原子个数为3+6×1/2+3=9;该晶体的密度为![]() 。
。

 名校课堂系列答案
名校课堂系列答案【题目】下列项目判断,结论正确的是
选项 | 项目 | 结论 |
A | 三种有机化合物:乙烷、氯乙烯、苯 | 分子内所有原子均在同一平面上 |
B | C4H8Cl2的同分异构体数目(不考虑立体异构) | 共有10种 |
C | 乙烯和苯都能使溴水褪色 | 褪色的原理相同 |
D | 由乙酸和乙醇制乙酸乙酯,油脂水解 | 均属于取代反应 |
A. A B. B C. C D. D

