题目内容
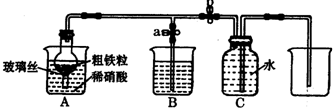
课外兴趣小组设计图所示装置,用粗铁粒与密度为1.89g?mL-1(质量分数为5%)的硝酸反应制取NO气体.请回答有关问题.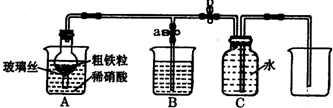
(1)密度为1.89g?mL-1的硝酸的物质的量浓度为______.
(2)NO气体能用排水法收集,而不能用排空气法收集的可能原因是______.
(3)当打开止水夹a,关闭止水夹b时,A装置的干燥管中观察到的现象是______.当A装置中气体几乎无色时,打开止水夹b,关闭止水夹a,可用C装置收集NO气体.
(4)完全反应后,A装置烧杯里含铁元素的价态可能是+2价或+3价或+2价和+3价.现有仪器和药品:试管和胶头滴管,0.1mol?L-1KSCN溶液、0.1mol?L-1KI溶液、0.2mol?L-1酸性KMnO4溶液、氯水等.请设计一个简单实验,探究上述判断,填写下列实验报告:
| 实验步骤 | 操作 | 现象与结论 |
| 第一步 | 取少量液体装于试管,向试管中滴入几滴KSCN溶液 | ______ |
| 第二步 | ______ | 若溶液紫色褪去,则说明含有Fe2+,若无明显变化,则说明不含Fe2+ |
解:(1)该硝酸的浓度为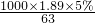 mol/L=1.5mol/L.
mol/L=1.5mol/L.
故答案为:1.5mol/L.
(2)NO密度与空气接近,且能与空气中氧气反应,NO不溶于水,故不能用排空气法收集,用排水法收集.
故答案为:NO密度与空气接近,且能与空气中氧气反应.
(3)铁与稀硝酸反应生成NO,NO在液面上部与氧气反应生成二氧化氮,气体由无色变为红棕色,同时金属溶解.
故答案为:有无色气体生成,逐渐变为红棕色,同时金属溶解.
(4)取溶液滴入KSCN溶液,溶液变红说明含有Fe3+,溶液不变红色说明不含Fe3+.
取溶液少许于试管内,滴加几滴酸性高锰酸钾溶液,若溶液紫色褪去,说明含有Fe2+,若无明显变化,则说明不含Fe2+.
故答案为:溶液变红说明含有Fe3+,溶液不变红色说明不含Fe3+;取溶液少许于试管内,滴加几滴酸性高锰酸钾溶液.
分析:(1)根据c=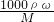 计算该硝酸的浓度.
计算该硝酸的浓度.
(2)NO密度与空气接近,且能与氧气反应.
(3)铁与稀硝酸反应生成NO,NO在液面上部与氧气反应生成二氧化氮.
(4)取溶液滴入KSCN溶液,溶液变红说明含有Fe3+,否则不含Fe3+.
加入氧化性的物质,溶液紫色,应加入酸性高锰酸钾.
点评:考查硝酸的性质、对实验原理装置的理解、方案设计、物质的量浓度计算等,难度中等,是对硝酸性质的综合考查,需要学生具有运用知识解决问题的能力.
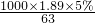 mol/L=1.5mol/L.
mol/L=1.5mol/L.故答案为:1.5mol/L.
(2)NO密度与空气接近,且能与空气中氧气反应,NO不溶于水,故不能用排空气法收集,用排水法收集.
故答案为:NO密度与空气接近,且能与空气中氧气反应.
(3)铁与稀硝酸反应生成NO,NO在液面上部与氧气反应生成二氧化氮,气体由无色变为红棕色,同时金属溶解.
故答案为:有无色气体生成,逐渐变为红棕色,同时金属溶解.
(4)取溶液滴入KSCN溶液,溶液变红说明含有Fe3+,溶液不变红色说明不含Fe3+.
取溶液少许于试管内,滴加几滴酸性高锰酸钾溶液,若溶液紫色褪去,说明含有Fe2+,若无明显变化,则说明不含Fe2+.
故答案为:溶液变红说明含有Fe3+,溶液不变红色说明不含Fe3+;取溶液少许于试管内,滴加几滴酸性高锰酸钾溶液.
分析:(1)根据c=
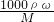 计算该硝酸的浓度.
计算该硝酸的浓度.(2)NO密度与空气接近,且能与氧气反应.
(3)铁与稀硝酸反应生成NO,NO在液面上部与氧气反应生成二氧化氮.
(4)取溶液滴入KSCN溶液,溶液变红说明含有Fe3+,否则不含Fe3+.
加入氧化性的物质,溶液紫色,应加入酸性高锰酸钾.
点评:考查硝酸的性质、对实验原理装置的理解、方案设计、物质的量浓度计算等,难度中等,是对硝酸性质的综合考查,需要学生具有运用知识解决问题的能力.

练习册系列答案
相关题目
课外兴趣小组设计图所示装置,用粗铁粒与密度为1.89g?mL-1(质量分数为5%)的硝酸反应制取NO气体.请回答有关问题.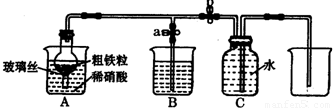
(1)密度为1.89g?mL-1的硝酸的物质的量浓度为______.
(2)NO气体能用排水法收集,而不能用排空气法收集的可能原因是______.
(3)当打开止水夹a,关闭止水夹b时,A装置的干燥管中观察到的现象是______.当A装置中气体几乎无色时,打开止水夹b,关闭止水夹a,可用C装置收集NO气体.
(4)完全反应后,A装置烧杯里含铁元素的价态可能是+2价或+3价或+2价和+3价.现有仪器和药品:试管和胶头滴管,0.1mol?L-1KSCN溶液、0.1mol?L-1KI溶液、0.2mol?L-1酸性KMnO4溶液、氯水等.请设计一个简单实验,探究上述判断,填写下列实验报告:

(1)密度为1.89g?mL-1的硝酸的物质的量浓度为______.
(2)NO气体能用排水法收集,而不能用排空气法收集的可能原因是______.
(3)当打开止水夹a,关闭止水夹b时,A装置的干燥管中观察到的现象是______.当A装置中气体几乎无色时,打开止水夹b,关闭止水夹a,可用C装置收集NO气体.
(4)完全反应后,A装置烧杯里含铁元素的价态可能是+2价或+3价或+2价和+3价.现有仪器和药品:试管和胶头滴管,0.1mol?L-1KSCN溶液、0.1mol?L-1KI溶液、0.2mol?L-1酸性KMnO4溶液、氯水等.请设计一个简单实验,探究上述判断,填写下列实验报告:
| 实验步骤 | 操作 | 现象与结论 |
| 第一步 | 取少量液体装于试管,向试管中滴入几滴KSCN溶液 | ______ |
| 第二步 | ______ | 若溶液紫色褪去,则说明含有Fe2+,若无明显变化,则说明不含Fe2+ |