题目内容
【题目】(I)写出下列物质在水中的电离方程式:
⑴氢氧化钡 ;
⑵碳酸钠: ;
写出下列反应的化学方程式:
⑶氯气与氢氧化钠溶液反应: ;
⑷向氯化镁溶液在加入澄清石灰水:
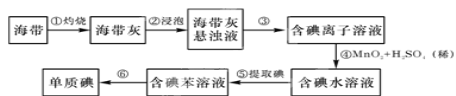
(II) 海带中含有丰富的碘。为从海带中提取碘,某研究性学习小组设计进行了以下实验:
⑴步骤③的实验操作名称是 需要的玻璃仪器有烧杯、玻璃棒和
⑵步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是 ;
⑶步骤①将海带放入___________(填仪器名称)中,用酒精灯充分加热灰化;
步骤②为了加速溶解的措施有 (任写一种合理措施)
⑷步骤⑤中某学生选择用苯从碘的水溶液中提取碘的理由是:____________、_______________。
【答案】(I)(I)(1)Ba(OH)2=Ba2++2OH-;
(2)Na2CO3=2Na++CO32-;
(3)Cl2+2NaOH=NaCl+NaClO+H2O;
(4)MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓;
(II)(1)过滤;漏斗(2)蒸馏
(3)坩埚;充分搅拌(或加热、用热水溶解等合理均可以)
(4)苯与水互不相溶,碘在苯中的溶解度比在水中的溶解度大得多
【解析】
试题分析:(I)(1)氢氧化钡是强电解质,电离方程式为Ba(OH)2=Ba2++2OH-;
(2)碳酸钠是强电解质,电离方程式为Na2CO3=2Na++CO32-;
(3)氯气与氢氧化钠溶液反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O;
(4)氯化镁溶液与澄清石灰水反应的化学方程式为MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓;
(II)(1)步骤③中除去不溶性固体,其实验操作名称是过滤,需要的玻璃仪器有烧杯、玻璃棒和漏斗;
(2)步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是蒸馏;
(3)固体灼烧在坩埚中,因此步骤①将海带放入坩埚,用酒精灯充分加热灰化;步骤②为了加速溶解的措施有充分搅拌(或加热、用热水溶解等合理均可以);
(4)步骤⑤中某学生选择用苯从碘的水溶液中提取碘的理由是苯与水互不相溶,碘在苯中的溶解度比在水中的溶解度大得多。
