题目内容
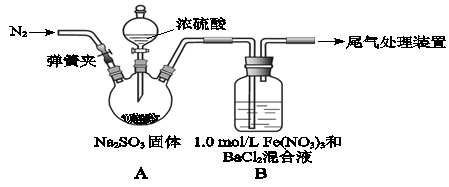
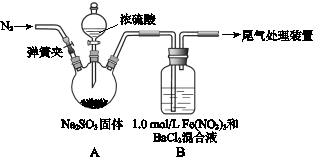
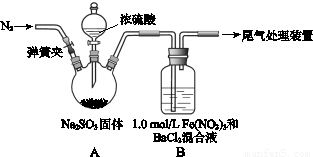
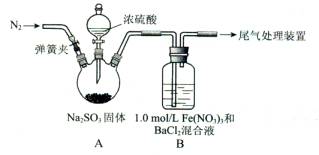
某研究小组探究SO2和Fe(NO3)3溶液的反应.
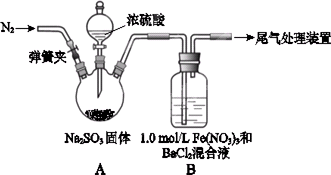
已知:1.0 mol/L的Fe(NO3)3溶液中c(H+)=0.01 mol/L
请回答:
(1)装置A中反应的化学方程式是________.
(2)为排除空气对实验的干扰,滴加浓硫酸之前应进行的操作是________.
(3)装置B中产生了白色沉淀,其成分是________,说明SO2具有________性.
(4)分析B中产生上述白色沉淀的原因可能是:
观点1:________;
观点2:SO2与Fe3+反应;
观点3:在酸性条件下SO2与NO3-反应;
①如果观点2正确,装置B中反应的离子方程式是________.
②如果想验证观点3,只需将装置B中的Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验.应选择的试剂是(填序号)________.
a.0.1 mol/L稀硝酸
b.1.5 mol/L Fe(NO3)2溶液
c.6.0 mol/L NaNO3和0.02 mol/L盐酸等体积混合的溶液
答案:

练习册系列答案
相关题目