题目内容
某有机物A由C、H、O三种元素组成,相对分子质量为90.将9.0g A完全燃烧的产物依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g.A能与NaHCO3溶液发生反应,且2分子A之间脱水只能生成六元环化合物.
(1)求A的分子式(要求有计算过程);
(2)写出六元环化合物的结构简式.
(1)求A的分子式(要求有计算过程);
(2)写出六元环化合物的结构简式.
分析:(1)浓硫酸增重5.4g为燃烧生成的水,碱石灰增重13.2g为燃烧产生的二氧化碳,根据n=
计算二氧化碳、水的物质的量,进而计算n(C)、n(H),根据质量守恒计算m(O),再计算n(O),结合相对分子质量确定A的分子式;
(2)A能与NaHCO3溶液发生反应,A中含有-COOH,且2分子A之间脱水只能生成六元环化合物,可能还含有-OH,结合A的分子式判断A的结构简式,进而确定六元环化合物的结构简式.
| m |
| M |
(2)A能与NaHCO3溶液发生反应,A中含有-COOH,且2分子A之间脱水只能生成六元环化合物,可能还含有-OH,结合A的分子式判断A的结构简式,进而确定六元环化合物的结构简式.
解答:解:(1)n(CO2)=
=0.3 mol,则n(C)=0.3 mol,
n(H2O)=
=0.3 mol,则n(H)=0.6 mol,
故n(O)=
=0.3mol,
故A的最简式为N(C):N(H):N(O)=1:2:1,A的相对分子质量为90,故A的分子式为C3H6O3,
答:A的分子式为C3H6O3.
(2)A能与NaHCO3溶液发生反应,A中含有-COOH,且2分子A之间脱水只能生成六元环化合物,A中还含有1个羟基-OH,形成六元环化合物的结构简式为: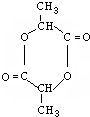 ,
,
答:形成六元环化合物的结构简式为: .
.
| 13.2g |
| 44g/mol |
n(H2O)=
| 5.4g |
| 18g/mol |
故n(O)=
| 9g-0.3mol×12g/mol-0.6mol×1g/mol |
| 16g/mol |
故A的最简式为N(C):N(H):N(O)=1:2:1,A的相对分子质量为90,故A的分子式为C3H6O3,
答:A的分子式为C3H6O3.
(2)A能与NaHCO3溶液发生反应,A中含有-COOH,且2分子A之间脱水只能生成六元环化合物,A中还含有1个羟基-OH,形成六元环化合物的结构简式为:
 ,
,答:形成六元环化合物的结构简式为:
 .
.点评:本题考查有机物分子式与结构式的确定,难度中等,根据守恒确定分子式是关键,注意掌握官能团的性质与原子守恒判断有机物的分子式方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
