��Ŀ����
����������(Mn2O3)���ִ���ҵ��λ�ù㷺��������ӵ�ص��Ʊ�������Ҫ�����á� �����̿� (��Ҫ�ɷ�ΪMnO2)�����̿�(��Ҫ�ɷ�ΪMnS)�Ʊ��ߴ���Mn2O3�Ĺ���������ͼ��ʾ��
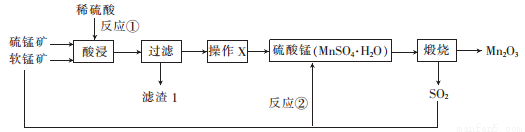
��1�� ��Ӧ���л�����һ�ַǽ������ʣ���÷ǽ���������___________���÷�Ӧ�Ļ�ԭ����__________�����ѧʽ��
��2�� ����XΪ����Ũ����_____________�����ˡ�ϴ�Ӻ�ɡ���ϴ�Ӳ����У����þƾ�ϴ��MnSO4 •H2O���壬��ҪĿ����______________��
��3�� Mn2O3��MnO2���ƣ�����ʱҲ����Ũ���ᷴӦ�ų�Cl2���÷�Ӧ�����ӷ���ʽΪ__________��
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�1Lij�����Һ�п��ܺ��е��������±���
���ܴ������е������� | H+��NH4+ ��Al3+��K+ |
���ܴ������е������� | C |
��1��������Һ����μ���NaOH��Һ���ʵ����ȣ�������������������ʵ�����n�������NaOH��Һ�������v���Ĺ�ϵ��ͼ��ʾ��

�������Һ��ȷ�����е������� ��
�ڲ���ȷ���Ƿ��е��������� ��
��Ҫȷ������ڿɲ�������ʵ���� ��
�ܿ϶������ڵ��������� ��
��2������⣬����Һ�к��д�����Cl����Br����I��������1L�û����Һ��ͨ��һ������Cl2����Һ��Cl����Br����I�������ʵ�����ͨ��Cl2���������״�����Ĺ�ϵ���±���ʾ��������ش��������⣺
Cl2���������״���� | 2.8L | 5.6L | 11.2L |
n��Cl���� | 1.25mol | 1.5mol | 2mol |
n��Br���� | 1.5mol | 1.4mol | 0.9mol |
n��I���� | a mol | 0 | 0 |
�ٵ�ͨ��Cl2�����Ϊ2.8Lʱ����Һ�з�����Ӧ�����ӷ���ʽΪ ��
��ԭ��Һ��Cl����Br����I�������ʵ���Ũ��֮��Ϊ ��


 Cd��2NiO(OH)��2H2O
Cd��2NiO(OH)��2H2O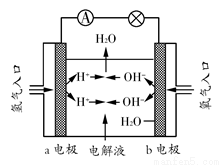
 NH3(g)+HI(g)��
NH3(g)+HI(g)�� PCl3(g)+Cl2(g) ��H>0,������������˵����Ӧ�Ѵﵽ��ѧƽ��״̬����
PCl3(g)+Cl2(g) ��H>0,������������˵����Ӧ�Ѵﵽ��ѧƽ��״̬���� l����Br����I����ClO����AlO2��
l����Br����I����ClO����AlO2��