题目内容
(12分)
|
实验曲线如右图(MgCO4的分解温度比CaCO2
低)
①700℃(即B点)对剩余固体的主要成分为
(填化学式)。
②该白云石中MgCO3的质量分数为
(保留3位有效数字)。
(2)乙同学利用滴定法测定白云石中MgCO3的含量。已知:①滴定时,EDTA分别有Ca2+或Mg2+以物质的量之比1:1进行反应,可用K—B指示剂作为该滴定反应的指示剂;②实验条件下。Mg2+开始沉淀时的pH为10,沉淀完全时的pH为11.2,Ca2+开始沉淀时的pH为12。
步骤1:准确称取白云石试样m g,在烧杯中用适量稀盐酸完全溶解;
步骤2:冷却后全部转移到250mL容量瓶中定容,
步骤3:从容量瓶中移取试液25.00mL,用NaOH溶液调节溶液pH约为9.5;
步骤4:加入2滴K—B指示剂,以c mol/L的EDTA标准溶液滴定至终点,消耗EDTA溶液V1mL;
步骤5:再从容量瓶中移取试液25.00mL, ;
步骤6:加入2滴K—B指示剂,继续以c mol/L的EDTA标准溶液滴定至终点,消耗EDTA溶液V2mL。
①根据上述分析数据,测得该白云石试样中MgCO3的质量分数为 (用含字母的代数式表示)。
②配制100mL c mol/L EDTA标准溶液,需要用到的玻璃仪器有烧杯、玻璃棒、量筒,
。
(12分)
(1)①MgO和CaCO3(2分) ②43.3%或0.433(2分)
(2)用NaOH溶液调节pH至11.2~12之间(3分)
①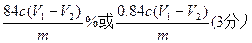 ②100mL量瓶 胶头滴管(2分)
②100mL量瓶 胶头滴管(2分)
解析

练习册系列答案
相关题目
白云石的主要成分为CaCO3·MgCO3,还含有少量Fe、Si的化合物。实验室以白云石为原料制备Mg(OH)2及CaCO3。步骤如下: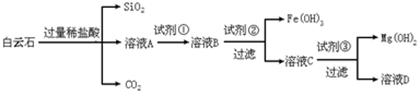
实验过程中需要的数据见下表:
| | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Mg2+ | 9.5 | 11.0 |
请回答下列问题:
(1)溶液A中含有Ca2+、Mg2+、Fe2+、Fe3+,则试剂①可选择_________(填字母,下同);试剂②可选择_________;试剂③可选择_________。
| A.KMnO4 | B.Cl2 | C.MgO | D.CaO |
(3)根据表中提供的数据判断,Fe(OH)3、Fe(OH)2和Mg(OH)2的溶度积常数由小到大的排列顺序为________________________________。
(4)将制取的Mg(OH)2煅烧得到MgO,然后在还原炉(真空)中,1200℃条件下,用硅铁(铁不参与反应)还原生成镁蒸气。在还原过程中反应温度对生成金属镁的影响如下图:
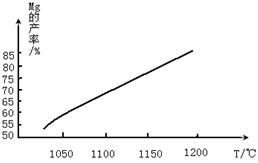
煅烧Mg(OH)2所需要的仪器除三角架、酒精灯外,还必须选择___________。MgO与硅铁发生的反应达到平衡后,平衡常数表达式为_______________________。由图可知,还原反应的△H ____0(填“>”或“<”)。
白云石的主要成分为CaCO3、MgCO3,还含有少量Fe、Si的化合物,实验室以白云石为原料制Mg(OH)2及CaCO3。步骤如下:

实验过程中需要的数据见下表:
|
|
氢氧化物开始沉淀时的pH |
氢氧化物沉淀完全时的pH |
|
Fe3+ |
1.9 |
3.2 |
|
Fe2+ |
7.0 |
9.0 |
|
Mg2+ |
9.5 |
11.0 |
请回答下列问题:
(1)过滤中所需的玻璃仪器是 。溶液A中含有Ca2+,Mg2+,Fe2+,Fe3+,则试剂①可选择
(填字母)
A.KMnO4 B.Cl2 C.H2O2
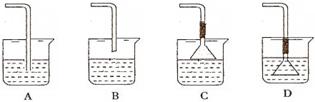
(2)若要利用反应过程中生成的CO2,从溶液D中制取CaCO3,需要先通入的一种气体是 ,然后通入CO2。通入CO2气体时请把右边的装置图补充完整(不允许更换溶液,导气管以下连接的仪器自选)。
(3)根据表中提供的数据判断,Fe(OH)3、Fe(OH)2和Mg(OH)2的溶度积常数由小到大的排列顺序为 。

(4)若将制取的Mg(OH)2:加入到某聚乙烯树脂中,树脂可燃性大大降低,Mg(OH)起阻燃作用的主要原因是 。
白云石的主要成分为CaCO3?MgCO3,还含有少量Fe、Si的化合物.实验室以白云石为原料制备Mg(OH)2及CaCO3.步骤如下:

实验过程中需要的数据见下表:
请回答下列问题:
(1)过滤中所需的玻璃仪器是 ,溶液A中含有Ca2+、Mg2+、Fe2+、Fe3+,则试剂①可选择 (填字母,下同).
A.KMnO4 B.Cl2 C.H2O2
(2)若要利用反应过程中生成的CO2,从溶液D中制取CaCO3,需要先通入的一种气体是 ,然后通入CO2.通入CO2气体时请把装置图补充完整 (不允许更换溶液,导气管以下连接的仪器自选)
(3)根据表中提供的数据判断,Fe(OH)3、Fe(OH)2和Mg(OH)2的溶度积常数由小到大的排列顺序为 .
(4)若将制取的Mg(OH)2加入到某聚乙烯树脂中Mg(OH)2,树脂可燃性大大降低,Mg(OH)2起阻燃作用的主要原因是 .


实验过程中需要的数据见下表:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Mg2+ | 9.5 | 11.0 |
(1)过滤中所需的玻璃仪器是 ,溶液A中含有Ca2+、Mg2+、Fe2+、Fe3+,则试剂①可选择 (填字母,下同).
A.KMnO4 B.Cl2 C.H2O2
(2)若要利用反应过程中生成的CO2,从溶液D中制取CaCO3,需要先通入的一种气体是 ,然后通入CO2.通入CO2气体时请把装置图补充完整 (不允许更换溶液,导气管以下连接的仪器自选)
(3)根据表中提供的数据判断,Fe(OH)3、Fe(OH)2和Mg(OH)2的溶度积常数由小到大的排列顺序为 .
(4)若将制取的Mg(OH)2加入到某聚乙烯树脂中Mg(OH)2,树脂可燃性大大降低,Mg(OH)2起阻燃作用的主要原因是 .




