题目内容
在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11。若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是( )
| A.1∶9 | B.1∶1 | C.1∶2 | D.1∶4 |
D
解析

下列说法正确的是( )
| A.常温下醋酸分子不可能存在于pH>7的碱性溶液中 |
| B.常温下向氯化铵溶液中加入少量氨水使溶液的pH=7,则混合溶液中c(Cl-)>c(NH4+) |
| C.0.1 mol/L的氯化铵溶液与0.05 mol/L的氢氧化钠溶液等体积混合,溶液中离子浓度c(Cl-)>c(NH4+)>c(Na+)>c(OH-) |
| D.0.1 mol·L-1硫化钠溶液中离子浓度关系c(OH-)=c(H+)+c(HS-)+c(H2S) |
下列说法正确的是
| A.c(H+)>c(OH一)的溶液一定显酸性 |
| B.常温下,pH=6的溶液一定是酸溶液 |
| C.电解稀硫酸或氢氧化钠溶液的产物不同 |
| D.水电解生成氢气和氧气,证明水是弱电解质 |
醋酸溶液中存在电离平衡:CH3COOH H++CH3COO-下列叙述不正确的是( )
H++CH3COO-下列叙述不正确的是( )
| A.醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-) |
| B.0.10 mol·L-1的CH3COOH溶液加水稀释,溶液中c(OH-)减小 |
| C.CH3COOH溶液中加入少量的CH3COONa固体,平衡逆向移动 |
| D.常温下,pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7 |
用0.102 6 mol·L-1的盐酸滴定25.00 mL未知浓度的氢氧化钠溶液,滴定达终点时,滴定管中的液面如下图所示,正确的读数为( )
| A.22.30 mL | B.22.35 mL | C.23.65 mL | D.23.70 mL |
已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下:
(1)CuSO4+Na2CO3
主要:Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑
次要:Cu2++CO32-=CuCO3↓(几乎不发生反应。下同)
(2)CuSO4+Na2S
主要:Cu2++S2-=CuS↓
次要:Cu2++S2-+2H2O=Cu(OH)2↓+H2S↑
则下列几种物质的溶解度大小的比较中,正确的是( )
| A.CuS<Cu(OH)2<CuCO3 |
| B.CuS>Cu(OH)2>CuCO3 |
| C.Cu(OH)2>CuCO3>CuS |
| D.Cu(OH)2<CuCO3<CuS |
下列反应不属于水解反应或水解方程式不正确的是( )
①HCl+H2O H3O++Cl-
H3O++Cl-
②AlCl3+3H2O=Al(OH)3+3HCl
③Na2CO3+2H2O H2CO3+2NaOH
H2CO3+2NaOH
④碳酸氢钠溶液:HCO3-+H2O CO32-+H3O+
CO32-+H3O+
⑤NH4Cl溶于D2O中:NH4++D2O NH3·D2O+H+
NH3·D2O+H+
| A.①②③④ | B.①②③ |
| C.①②⑤ | D.全部 |
有四种物质的量浓度相等、且都由一价阳离子A+和B+及一价阴离子X-和Y-组成的盐
溶液。据测定常温下AX和BY溶液的pH=7,AY溶液的pH>7,BX溶液的pH<7,由此判断不水解的盐是( )
| A.BX | B.AX | C.AY | D.BY |
常温下,向100 mL 0.1 mol·L-1 H2A(二元酸)溶液中逐滴加入0.2 mol·L-1 NaOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。下列有关说法正确的是( )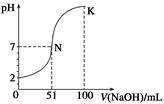
| A.H2A为二元强酸 |
| B.N点对应溶液有:c(Na+)=c(A2-)+c(HA-) |
| C.K点对应溶液中离子浓度由大到小的顺序为c(A2-)>c(Na+)>c(OH-)>c(H+) |
| D.K点时加水稀释溶液,c(H+)增大 |