题目内容
(5分)胃酸是由胃黏膜的壁细胞分泌的,实际上就是盐酸。正常人的胃液中盐酸浓度大约为0.1 mol·L-1,每日分泌胃酸2 L左右。某胃酸过多患者经测定盐酸浓度为0.126 mol·L-1。医生建议该患者服用Stomachee,按说明书要求服用即可。如图是该药品的标签,根据你所学的化学知识,通过计算回答正常服用此药物能否使该患者的胃酸恢复正常?

正常服用此药物不能使该患者的胃酸恢复正常。
患者每日的盐酸超标量为n(HCl)=(0.126 mol·L-1-0.1 mol·L-1)×2 L=0.052 mol,每日摄入Mg(OH)2的质量为1片×3×0.25 g/片=0.75 g,根据中和胃酸的化学方程式:Mg(OH)2+2HCl===MgCl2+2H2O可知,消耗0.052 mol HCl需Mg(OH)2的质量为58 g·mol-1×0.052 mol×=1.508 g。因为1.508 g>0.75 g,故正常服用此药物不能使该患者的胃酸恢复正常。

练习册系列答案
相关题目
 的化学性质相同
的化学性质相同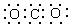 ④3—甲基丁烷 ⑤坩锅钳 ⑥乙稀
④3—甲基丁烷 ⑤坩锅钳 ⑥乙稀 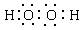 ⑧三角椎形 ⑨溶量瓶 ⑩银铵溶液
⑧三角椎形 ⑨溶量瓶 ⑩银铵溶液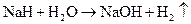 ,它也能跟液氨、乙醇等发生类似的反应,并都产生氢气,下列有关NaH的叙述错误的是( )
,它也能跟液氨、乙醇等发生类似的反应,并都产生氢气,下列有关NaH的叙述错误的是( )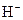 半径比
半径比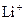 半径小
半径小 生成
生成