题目内容
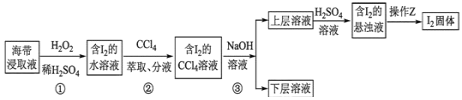
【题目】为了从海带浸取液中提取碘,某同学设计了如图实验方案:下列说法正确的是( )
A.①中反应的离子方程式:![]()
B.②中分液时含![]() 的
的 ![]() 溶液从分液漏斗上口倒出
溶液从分液漏斗上口倒出
C.③操作使用的是反萃取法,得到的上层溶液中含有![]()
D.操作Z 的名称是蒸发
【答案】C
【解析】
海带浸取液中的碘离子被加入的过氧化氢氧化得到含碘单质的水溶液,加入四氯化碳振荡、静置分层、分液得到碘单质的四氯化碳溶液,向碘单质的四氯化碳溶液中加入氢氧化钠溶液,碘单质和氢氧化钠反应得碘化钠和次碘酸钠溶液,振荡、静置分层,去掉四氯化碳层,再加入稀硫酸酸化,碘化钠和次碘酸钠在酸性条件下发生氧化还原反应得到碘单质的悬浊液,通过过滤得到碘单质。
A.反应为酸性环境,I-被H2O2氧化成I2,①中反应的离子方程式:2I+2H++H2O2═I2+2H2O,A错误;
B.四氯化碳的密度比水大,在下层,②中分液时I2的CCl4溶液从分液漏斗下口放出,B错误;
C.③中反应为I2+2OH=IO+I+H2O,加入的NaOH溶液将I2从CCl4中反萃取得到IO和I的水溶液,CCl4密度比水大,IO和I的水溶液在上层,C正确;
D.含I2的悬浊液得到固体I2应为过滤,D错误。
答案选C。

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目



