题目内容
工业上以黄铜矿(主要成分CuFeS2)为原料制备CuSO4·5H2O的主要流程如下:

(1)下列装置不能用于吸收气体X的是_____________(填代号)。

(2)熔渣Y的成分为Fe2O3和FeO,选用提供的试剂,设计实验验证熔渣中含有FeO。写出有关实验操作、现象与结论。
提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMn04溶液、NaOH溶液、氯水。 。
(3)向粗铜中加 入硫酸和硝酸的混酸溶液制取硫酸铜时(杂质不参加反应),混酸中HNO3与H2SO4的最佳物质的量之比为
入硫酸和硝酸的混酸溶液制取硫酸铜时(杂质不参加反应),混酸中HNO3与H2SO4的最佳物质的量之比为
(4)用滴定法测定所得产品中CuSO4.5H2O的含量,称取ag样品配成100 mL溶液,取出2 0.00 mL,用c mol.L-l滴定剂EDTA( H2Y2-)标准溶液滴定至终点(滴定剂不与杂质反应),消耗滴定剂bmL。滴定反应如下:Cu2++ H2Y2
0.00 mL,用c mol.L-l滴定剂EDTA( H2Y2-)标准溶液滴定至终点(滴定剂不与杂质反应),消耗滴定剂bmL。滴定反应如下:Cu2++ H2Y2 -= CuY2-+ 2H+,则CuSO4·5H2O质量分数为_____________。滴定管用
-= CuY2-+ 2H+,则CuSO4·5H2O质量分数为_____________。滴定管用 蒸馏水洗涤后,直接注入标准溶液,则会导致测定结果偏 。(填“偏高”、“偏低”和“无影响”)
蒸馏水洗涤后,直接注入标准溶液,则会导致测定结果偏 。(填“偏高”、“偏低”和“无影响”)
硫酸及其盐在工农业生产中有着重要的应用。
(1)SO2催化氧化为SO3的反应是工业制硫酸的重要过程,①下图是反应过程中SO2和SO3的浓度隨时间t的变化情况。反应从开始到达到平衡时,用O2表示的平均反应速率为 。
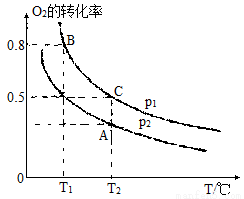
②在一容积可变的密闭容器中充入一定量SO2(g)和O2(g),O2的平衡转化率如图所示。则p1与p2的大小关系是p1 p2 (填“>”“<”或“=”);A、B、C三点的平衡常数大小关系为 (用Ka、Kb、Kc表示三点对应的平衡常数)。
(2)生产硫酸过程中产生的尾气,可用氨水吸收,溶液中生成(NH4)2SO4、(NH4)2SO3等溶质。
①(NH4)2SO4溶液呈酸性的原因是 (用离子方程式表示)。
②己知:
NH3·H2O | H2SO3 | |
电离平衡常数 | 1.7×10—5 | Ka1=1.54×10—2 Ka2=1.02×10—7 |
NH4HSO3溶液呈 (填“酸性”、“碱性”、“中性”)。
③25℃时,相同物质的量的SO2与NH3溶于水,所得溶液中c(H+)—c(OH—)= (填序号)。
A.c(SO32—)—c(H2SO3)
B.c(HSO3—)+c(SO32—)—c(NH4+)
C.c(SO32—)+c(NH3·H2O)—c(H2SO3)
D.(HSO3—)+2c(SO32—)—c(NH4+)
(3)己知:①BaSO4(s)+4C(s)=BaS(s)+4CO(g) △H=+571.2kJ•mo1—1
②BaS(s)=Ba(s)+S(s) △H=+460kJ•mo1—1
③2C(s)+O2(g)=2CO(g) △H=—221kJ•mo1—1
则用Ba(s)、S(s)、O2(g)反应生成BaSO4(s)的热化学方程式为 。


 原,是还原剂
原,是还原剂